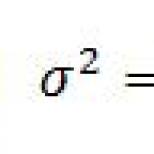Что такое коррозия металлов в химии. Коррозионные свойства металлов. Количественная оценка скорости коррозии
Омский государственный технический университетКафедра «Химия»
Новгородцева Л.В.
ОБЩАЯ ХИМИЯ
Химические свойства металлов.
Коррозия металлов.
Лекция
Мультимедийная слайд-лекция
©ОмГТУ, 2014
Распространение металлов в природе
МЕТАЛЛЫ В ПРИРОДЕ. КЛАРК.
Клаа́рковое числоа́ (или кларки элементов, ещё чаще говорятпросто кларк элемента) - числа, выражающие среднее
содержание химических элементов в земной
коре, гидросфере, Земле, космических
телах, геохимических или космохимических системах и др.,
по отношению к общей массе этой системы.
Выражается в % или г/кг.
Наиболее
распространены из
металлов в земной
коре
Алюминий
Al –
8,45 % (масс.)
Железо
Fe -
4,4 % (масс.)
Кальций
Ca -
3,3 % (масс.)
Натрий
Na -
2,6 % (масс.)
Магний
Mg -
2,1 % (масс.)
Титан
Ti -
0,61 % (масс.)
НАИБОЛЕЕ РАСПРОСТРАНЕННЫЕ СОЕДИНЕНИЯ МЕТАЛЛОВ В ПРИРОДЕ
Из природных соединений металлов наиболеераспространенными являются оксиды.
Fe2O3 - гематит; Fe3O4 – магнитный железняк, магнетит;
Cu2O - куприт; Al2O3 - корунд; TiO2 – рутил, анатаз, брукит;
MnO2 - пиролюзит; SnO2 – касситерит и др.
Широко распространены сульфиды малоактивных
металлов: NiS; CuS; ZnS; PbS; FeS2.
В виде галидов:- фторидов, хлоридов - встречаются щелочные и
щелочноземельные металлы.
В виде карбонатов – легкие металлы - Mg, Ca (CaCO3).
В виде сульфатов – активные металлы Na, Ca, Ba, Mg (Na2SO4).
Растворимые соли металлов встречаются в воде океанов, морей, озер.
Получение металлов
Добывание металлов из руд
Большинство металлов находятся в природе в видесоединений с другими элементами, в основном в виде руд.
В свободном состоянии (самородки)
встречаются золото и платина, а
серебро и медь – отчасти; иногда
попадается самородная ртуть
некоторые другие металлы.
Au и Pt добывают посредством
механического отделения от породы,
в которой они заключены (например
промывкой), или путем извлечения
их из породы различными реагентами
с последующим выделением из
раствора
ПИРОМЕТАЛЛУРГИЯ
Получение металлов из руд ихвосстановлением при высоких
температурах
Восстановители
Углерод (кокс)
PbO + C = Pb + CO
Оксид углерода
(II)
Fe2O3 + 3CO = 2Fe + 3CO2
Водород
MnO2 + 2H2 = Mn + 2H2O
гидротермия
Более активный
металл
(металлотермия)
Fe2O3 + 2Al = 2Fe + Al2O3
алюмотермия
TiCl4 + 2Mg = Ti + 2MgCl2
магниетермия
карботермия
ГИДРОМЕТАЛЛУРГИЯ
Растворение природногосоединения в виде водных
растворов с помощью различных
реагентов с последующим
выделением металла из
раствора. Процесс идет при
обычных температурах.
Восстановители – активные
металлы или электроны
Из руд золото извлекают с помощью цианида калия, а
затем восстанавливают порошкообразным цинком
2K + Zn→ K2 + 2Au
Металл получают в мелкораздробленном состоянии
ЭЛЕКТРОМЕТАЛЛУРГИЯ
Электрометаллургия – получение металлов из водныхрастворов или расплавов с помощью электрического тока
(электролизом)
Электролиз водных растворов: для получения малоактивных металлов
CuSO4 + H2O→ Cu0 + H2SO4 + O2
Катод (-): Cu2+ + 2e- → Cu0
Анод (+): 2H2O - 4e- → O2 + 4Н+
Электролиз расплавов: для
получения активных металлов
2NaClрасплав→ 2Na0 + Cl20
Катод (-): Na+ + 1e- → Na0
Анод (+): 2Cl- - 2e- → Cl20
ФЛОТАЦИОННЫЙ МЕТОД
Флотация – метод основанный наразличной смачиваемости поверхности
минерала водою.
Пример: руду, состоящую из сернистого металла и пустой
породы, измельчают, заливают водой, прибавляя малополярное
органическое вещество (для образования пены) и небольшое
количество реагента «коллектора», который адсорбируется
поверхностью минерала. Через смесь снизу пропускают струю
воздуха. В результате частицы минерала со слоем молекул
«коллектора» прилипают к пузырькам воздуха, а частицы пустой
породы, смоченные водой, опускаются на дно. Затем пену
собирают, отжимают и получают руду с большим содержанием
металла.
МАГНИТНЫЙ СПОСОБ
Магнитная сепарация применяется для обогащения руд, содержащихминералы с относительно высокой магнитной восприимчивостью. К ним
относятся магнетит, франклинит, ильменит и пирротин, а также
некоторые другие минералы железа, поверхности которых могут быть
приданы нужные свойства путем низкотемпературного обжига.
Сепарация производится как в водной,
так и в сухой среде. Сухая сепарация
больше подходит для крупных зерен,
мокрая - для тонкозернистых песков и
шламов. Обычный магнитный сепаратор
представляет собой устройство, в котором
слой руды толщиной в несколько зерен
перемещается непрерывно в магнитном
поле. Магнитные частицы вытягиваются
из потока зерен лентой и собираются для
дальнейшей переработки; немагнитные
частицы остаются в потоке.
Природа химической связи в металлах
ОБЩИЕ ФИЗИЧЕСКИЕ СВОЙСТВА
Высокая электропроводность, высокая теплопроводность,пластичность, т.е. способность подвергаться деформации при
обычных и повышенных температурах, не разрушаясь.
Благодаря этому свойству металлы
поддаются ковке, прокатке,
вытягиванию в проволку (волочению),
штамповке.
Металлам присущи
также металлический
блеск, обусловленный
их способностью
хорошо отражать свет.
МЕТАЛЛЫ. ПОЛУПРОВОДНИКИ. ДИЭЛЕКТРИКИ. ЗОННАЯ ТЕОРИЯ.
МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
Способность электронов свободно передвигаться по кристаллуи переносить энергию из одной ее части в другую служит
причиной высокой тепло- и электропроводимости металлов
Валентные электроны, осуществляющие химическую связь,
принадлежат не двум или нескольким определенным атомам,
а всему кристаллу металла. При этом валентные электроны
способны свободно перемещаться в объеме кристалла.
Образованную таким образом
химическую связь называют
металлической связью.
Совокупность «свободных»
электронов в металле электронным газом
Химические свойства металлов
Стандартный водородный электрод
Для построения численной шкалы электродныхпотенциалов нужно потенциал какого-либо электродного
процесса принять равным нулю. В качестве эталона для
создания такой шкалы принят электродный процесс:
2Н+ +2е- = Н2
Водородный электрод
Платиновая пластина,
электролитически покрытая
губчатой платиной и погруженная
в 1М раствор серной кислоты,
через который барботируется
газообразный водород по
давлением 1 атмосфера.
На поверхности соприкосновения
платины с раствором кислоты
устанавливается равновесный
процесс:
2Н+ +2е- ⇆ Н2
ЭЛЕКТРОХИМИЧЕСКИЙ РЯД НАПРЯЖЕНИЯ МЕТАЛЛОВ
Потенциал водородного электрода воспроизводится с очень высокойточностью. Поэтому водородный электрод и принят в качестве
эталона при создании шкалы электродных потенциалов.
Для определения потенциала того
или иного электродного процесса
нужно составить гальванический
элемент
из
испытуемого
и
стандартного
водородного
электрода и измерить его ЭДС.
Поскольку потенциал стандартного
водородного электрода равен нулю,
то
измерение
ЭДС
будет
представлять
собою
потенциал
электродного процесса.
Таким образом получают электрохимический ряд напряжения
металлов. Т.к. измерения проводят относительно водородного
электрода этот ряд называют водородной шкалой.
ВОССТАНОВИТЕЛЬНЫЕ СВОЙСТВА. ЭНЕРГИЯ ИОНИЗАЦИИ
Ослабление восстановительных свойств, активностиЭтот ряд называется электрохимическим рядом напряжения
металлов. Энергия ионизации, определяется положением
металла в периодической системе. В электрохимическом
ряду напряжения металл, стоящий левее, может вытеснять
из растворов или расплавов солей металл, стоящий правее.
Пользуясь этим рядом, можно предсказать, как металл будет
себя вести в паре с другим.
В электрохимический ряд напряжения включен также
водород. Это позволяет сделать заключение о том, какие
металлы могут вытеснить водород из растворов кислот.
Так, например, железо вытесняет водород из растворов
кислот, так как находится левее его;
медь же не вытесняет водород, так как находится правее
его в ряду напряжения металлов.
АКТИВНОСТЬ МЕТАЛЛОВ В СООТВЕТСТВИИ С РЯДОМ НАПРЯЖЕНИЯ МЕТАЛЛОВ
Li, K, Ba, Na, La, Mg, Lu, Be, Sc, Ti, Hf, Al, Zr, V, Mn, Cr, Zn, Fe, Cd,Co, Mo, Sn, W, Pb, H
Ge, Sb, Bi, Cu, Re, Ag, Pd, Hg, Pt, Au.
Все металлы можно разделить на группы:
активные металлы стоят в ряду активности перед Cd;
средней активности – находятся в ряду от Cd до Н;
малоактивные металлы стоят в ряду активности после Н.
ОБЩИЕ ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
Химические свойства металлов определяются:строением их атомов,
типом кристаллической решетки.
Главное и наиболее общее свойство металлов – хорошие
восстановители, т.е. легко отдают электроны:
Ме0 - ne-→ Меn+
На основании ряда стандартных электродных потенциалов
можно сделать вывод о химической активности металлов
С солями более активный металл (стоящий левее в ряду
напряжения металлов) вытесняет менее активный из его
соли: Zn + CuCl2 → ZnCl2 + Cu
ОБЩИЕ СВОЙСТВА МЕТАЛЛОВ. ВЗАИМОДЕЙСТВИЕ С ПРОСТЫМИ ВЕЩЕСТВАМИ
МЕТАЛЛкислород
оксиды, пероксиды,
надпероксиды
галогены
фториды, хлориды,
бромиды, иодиды
сера
сульфиды
азот
нитриды
фосфор
фосфиды
водород
гидриды
углерод
карбиды
кремний
силициды
Взаимодействие металлов с водой
ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ВОДОЙ С ТЕРМОДИНАМИЧЕСКОЙ ТОЧКИ ЗРЕНИЯ
Взаимодействие металлов с водой идет по реакции:Ме0 + Н2О = МеОН + 1/2 H2
Ϥ0Red
Окислитель:
2H+ + 2e- → H2
Ϥ0Ох
Е= Ϥ0Ох - Ϥ0Red > 0
Ϥ0Ох > Ϥ0Red
Стандартный электродный потенциал ионов водорода в воде
(рН = 7):
Ϥ0Ох = -0,59.рН = -0,41 В
Поэтому условие восстановления металла водой можно
записать в виде:
Ϥ0Red < -0,41 В
Т.е. с водой, вытесняя из нее водород, взаимодействуют все
металлы, стоящие до Сd, стандартный электродный
потенциал которых ниже -0,41 В.
ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ВОДОЙ
Активные металлы (металлы от начала ряда активности до Mg) сводой дают гидроксиды и водород:
2Na + 2H2O = 2NaOH + H2
Металлы средней активности (от Mg до Н2) дают оксиды и
водород (при нагревании):
С горячей водой реагируют металлы стоящие в ряду от Mg до Cd:
Mg + 2H2O = Mg(OH)2 + H2
3Fe + 4H2O = Fe3O4 + 4H2
Температура реакции t = 100 °С
Температура реакции t = 700 °С
Некоторые из металлов, расположенные
между Mg и Cd, например, Zn, Al покрыты защитными окисными
плёнками (ZnO, Al2O3) и не растворяются в воде, т.е. металл не
активен (пассивен). Явление называется пассивацией металла.
Неактивные металлы с водой не реагируют.
Взаимодействие металлов с кислотами
ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ
Разбавленные кислоты являются окислителями за счетводорода
Восстановитель: Ме0 - ne-→ Меn+
Ϥ0Red
Окислитель:
2H+ + 2e- → H2
Ϥ0Ох = Ϥ0 2H+/H2 = 0
Е= Ϥ0Ох - Ϥ0Red > 0
Ϥ0Ох > Ϥ0Red
Ϥ0Red < 0 В
Mg0 + 2HСl → МgCl2 + H2
Металлы, находящиеся в ряду напряжения металлов до
водорода вытесняют его из кислот (исключения:
концентрированная серная кислота, азотная кислота любой
концентрации).
ПАССИВАЦИЯ МЕТАЛЛОВ КИСЛОТАМИ
Иногда образуются нерастворимые или малорастворимыепродукты, которые тормозят реакцию.
Например, свинец Pb не растворяется в разбавленной серной
кислоте и соляной, т.к. образуются PbSO4 и PbCl2, которые не
растворяются в воде и тормозят окисление.
Pb + 2HCl = PbCl2 + H2
Эффект пассивации из-за образования защитной пленки на
поверхности, приводящий к замедлению реакции,
наблюдаются у некоторых других металлов.
Чаще всего продукты образуются при взаимодействии со
следующими кислотами: H3PO4, H2SO3, H2CO3, HCN, HF.
ТАБЛИЦА РАСТВОРИМОСТИ
ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С КОНЦЕНТРИРОВАННОЙ СЕРНОЙ КИСЛОТОЙ
В концентрированной серной кислоте в роли окислителявыступает сера в степени окисления +6, входящая в
состав сульфат-иона SO42-.
Концентрированная серная кислота окисляет все
металлы, стандартный электродный потенциал которых
меньше 0,36 В, максимального значения электродного
потенциала в электродных процессах с участием сульфатиона SO42-.
Концентрированная серная кислота восстанавливается до
следующих продуктов
H2S+6O4 (к) → S+4O2 → S0 → H2S2-
ВЛИЯНИЕ АКТИВНОСТИ МЕТАЛЛОВ ПРИ ВЗАИМОДЕЙСТВИИ С КОНЦЕНТРИРОВАННОЙ СЕРНОЙ КИСЛОТОЙ
Активные металлы реагируют с кислотой, восстанавливая еедо сероводорода
5H2S6+O4(k) + 4Zn = 4ZnSO4 + H2S +4H2O
Малоактивные металлы реагируют с кислотой, восстанавливая
ее до SO2
2H2S6+O4(k) + Cu0 = CuSO4 + SO2 + 2H2O
Концентрированная серная кислота пассивирует металлы
средней активности: Fe, Be, Cr, Co, Al. На поверхности
металла образуются плотные пленки оксида:
3H2SO4(k) +2Fe = Fe2O3 + 3H2O +3SO2
Металлы Re, Mo, Tc, Ti, V взаимодействуют в соответствии с
уравнением
2V +5H2SO4(k) =2HVO3+5SO2 + 4H2O
ОКИСЛИТЕЛЬНАЯ СПОСОБНОСТЬ АЗОТНОЙ КИСЛОТЫ
Кислотный остаток азотной кислоты (любой концентрации)обладает высокой окислительной способностью.
В азотной кислоте в роли окислителя выступает азот в
степени окисления +5.
Восстанавливается кислота до следующих продуктов:
HN5+O3 → N4+O2 → N2+O → N+2O → N20 → N3-H3
Степень восстановления растет
Чем более концентрированная кислота тем более глубоко
она восстанавливается.
Характер продуктов реакции зависит как от концентрации
кислоты, так и от активности металла
ТЯЖЕЛЫЕ МЕТАЛЛЫ
Известнооколо
сорока
различных
определений
термина тяжелые металлы, и невозможно указать на одно из
них, как наиболее принятое.
Используемым критерием может быть атомный вес свыше
50,
к тяжелым металлам относят более 40 металлов
периодической системы Д.И. Менделеева: V, Cr, Mn, Fe, Co,
Ni, Cu, Zn, Mo, Cd, Sn, Hg, Pb, Bi и др.
Другим часто используемым критерием является плотность,
примерно равная или большая плотности железа (8 г/см3),
классификация Н. Реймерса: Pb, Cu, Zn, Ni, Cd, Co, Sb, Sn,
Bi, Hg.
Существуют классификации, основанные и на других
значениях пороговой плотности или атомного веса. Некоторые
классификации делают исключения для благородных и
редких металлов, не относя их к тяжелым, некоторые
исключают нецветные металлы (железо, марганец).
ВЗАИМОДЕЙСТВИЕ ТЯЖЕЛЫХ МЕТАЛЛОВ С АЗОТНОЙ КИСЛОТОЙ
В случае взаимодействия тяжелых металлов сконцентрированной азотной кислотой чаще всего
выделяется оксид азота (IV) NO2, с разбавленной – оксид
азота (II) NO.
HNO3(разб) + Cu0 → Cu(NO3)2 + NO + H2O
HNO3(конц) + Cu0 → Cu(NO3)2 + NO2 + H2O
В случае концентрированной азотной кислоты чаще всего
выделяется оксид азота (IV) NO2, в случае разбавленной –
оксид азота (II) NO.
ВЗАИМОДЕЙСТВИЕ ЩЕЛОЧНЫХ И ЩЕЛОЧНО-ЗЕМЕЛЬНЫХ МЕТАЛЛОВ С АЗОТНОЙ КИСЛОТОЙ
Концентрированная азотная кислота при взаимодействии сщелочными (элементы 1 группы главной подгруппы: Li, Na,
K, Rb, Cs, Fr) и щелочно-земельными металлами (элементы 2
группы главной подгруппы (кроме Be, Mg): Ca, Sr, Ba, Ra)
восстанавливается до оксида азота (I) N2O
HNO3(конц) + Ca0 → Ca+2(NO3)2 + N+2O + H2O
HNO3(разб) + Ca0 → N-3H4NO3 + Ca(NO3)2+ H2O
Разбавленная азотная кислота при взаимодействии с
щелочными, щелочно-земельными металлами, Zn, Fe
восстанавливается до нитрата аммония NH4NO3.
ВЛИЯНИЕ СТЕПЕНИ ОКИСЛЕНИЯ МЕТАЛЛА. ПАССИВАЦИЯ
В зависимости от химической природы металла отмечены следующиезакономерности:
металлы, у которых устойчива низкая степень окисления,
образуют соответствующие ионы:
Mg0 + HNO3 (разб) → Mg(NO3)2 + NO + H2O
металлы (W, Ti, V, Re, Tc), для которых наиболее характерна
высокая степень
кислоты:
окисления,
образуются
кислородсодержащие
W0 + 2HNO3 (разб) → H2WO4 + NO
W0 + 6HNO3 (конц) → H2WO4 + 6NO2 + 2H2O
3Tc + 7HNO3 (разб) → 3HTcO4 +7NO + 2H2O
Азотная кислота любой концентрации пассивирует
металлы: Fe, Cr, Al, Be, Bi, Ni на холоде.
Окислительная способность азотной кислоты усиливается
добавлением к ней фтороводородной
или хлороводородной кислот.
Эти смеси растворяют самые малоактивные металлы.
21HF + 5HN+5O3 + Ta → 3H2-2 + 5NO + 10H2O
«Царская водка» - смесь
концентрированных кислот HNO3
и HCl в соотношении 1:3.
Представляет из себя жидкость
желтого цвета с запахом хлора и
оксидов азота.
ВЗАИМОДЕЙСТВИЕ СО СМЕСЯМИ КИСЛОТ
«Царская водка» растворяет золото и платину. Действие ееобъясняется тем, что азотная кислота окисляет соляную
с
выделением свободного хлора и образованием хлористого
нитрозила N+3OCl:
HN+5O3 + 3HCl = Cl2 + N+3OCl + 2H2O
Хлористый нитрозил является промежуточным продуктом реакции и
разлагается:
2N+3OCl = 2NO + Cl2
Хлор в момент выделения состоит из атомов, что и обусловливает
Высокую окислительную способность царской водки.
Au+ HN+5O3 + 3HCl →AuCl3 + NO + 2H2O
3Pt+ 4HN+5O3 + 12HCl →3PtCl3 + 4NO + 8H2O
С избытком HCl хлорид золота (III) и хлорид платины (IV)
образуют комплексные соединения H и H2
Au+ HN+5O3 + 4HCl → H + NO + 2H2O
Взаимодействие металлов с водными растворами щелочей
ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ВОДНЫМИ РАСТВОРАМИ ЩЕЛОЧЕЙ
С растворами щелочей взаимодействуют металлысклонные к образованию анионных комплексов, т.е. те
металлы, у которых оксиды и гидроксиды имеют
амфотерный характер:
Это амфотерные металлы – Zn, Al, Be, Ga, Sn, Pb.
Механизм протекания реакции (окисление идет
за счет молекул воды):
Zn +2 H2O = Zn(OH)2↓ + H2
Zn(OH)2↓ +2 NaOH = Na2-2.
УСТОЙЧИВОСТЬ АНИОННЫХ КОМПЛЕКСОВ
Чем устойчивее комплексные анионы типа [Э(ОН)n]x-,тем легче идет реакция. Замечено, что такие анионы
наиболее
устойчивы
у
таких
металлов
как
цинк,
алюминий, бериллий, поэтому они легко растворяются
в водных растворах щелочей. Для железа, кобальта,
титана,
марганца
комплексы
медленно.
не
и
ряда
устойчивы
других
и
металлов
взаимодействие
такие
идет
ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ВЫСОКИМИ СТЕПЕНЯМИ ОКИСЛЕНИЯ С ВОДНЫМИ РАСТВОРАМИ ЩЕЛОЧЕЙ
Взаимодействуют со щелочами и некоторые d-элементы,которые в присутствии окислителей образуют соединения с
высокими степенями окисления. Ванадий, вольфрам, хром,
например,
в
расплавленных
щелочах
окисляются
кислородом в ванадаты – Me3VO4, в вольфраматы – Me2WO4
и в хроматы – Me2СrO4, соответственно:
2W + 4NaOH + 3O2 = 2Na2WO4 + 2 H2O
РАСТВОРЕНИЕ АЛЮМИНИЯ В ВОДНОМ РАСТВОРЕ ЩЕЛОЧИ
Алюминий с водой не взаимодействует, хотя является активнымметаллом. Причиной инертности алюминия является образование
на его поверхности под действием кислорода воздуха в обычных
условиях оксидной пленки Al2O3, обладающей очень сильным
защитным действием. Добавленная щелочь растворяет оксидную
пленку с образованием гидроксоалюмината и создает возможность
непосредственного взаимодействия алюминия с водой.
Реакция идет по схеме:
1.Al2O3 + 2NaOH + 3H2O → 2Na
2. 2Al + 6H2O → 2Al(OH)3 + 3H2
3. Al(OH)3 + NaOH → Na
Коррозия металлов
КОРРОЗИЯ МЕТАЛЛОВ.
Коррозия – этосамопроизвольно
протекающий
процесс разрушения
металла в
результате
взаимодействия с
окружающей средой.
МАТЕРИАЛЬНЫЕ ПОТЕРИ.
Материальные потери прикоррозии:
Разрушение трубопроводов,
металлических частей машин,
корпусов судов, морских
сооружений (более 10 %
ежегодной выплавки металлов
теряется из-за коррозии).
Стоимость потерянного
продукта через
прокорродированную систему
труб.
Простои предприятий на
период замены
металлических конструкций
подвергшихся коррозии.
МЕХАНИЗМ ПРОЦЕССА КОРРОЗИИ.
Процесс идет с выделением энергии и рассеивания вещества(энтропия системы возрастает ∆S > 0).
Получение металлов в чистом виде всегда сопровождается
затратой энергии.
Эта энергия накапливается в них как свободная энергия
Гиббса, и делает их химически активными веществами.
Металлургический процесс:
_
Коррозионный процесс:
_
Меn+ + ne → Me0
Me0 - ne → Меn+
∆G0х.р. >0
∆G0х.р. < 0
(идет с затратой энергии)
(самопроизвольный процесс)
КЛАССИФИКАЦИЯ ПРОЦЕССОВ КОРРОЗИИ.
КОРРОЗИЯ МЕТАЛЛОВХимическая коррозия металлов
СУЩНОСТЬ ХИМИЧЕСКОЙ КОРРОЗИИ.
Химическая коррозия характерна для сред, не проводящихэлектрический ток.
Сущность процесса химической коррозии сводится к
окислительно-восстановительным
реакциям,
причем
наблюдается непосредственный переход электронов металла
на окислитель.
Она представляет собой самопроизвольное разрушение
металлов в среде окислительного газа (O2, SO2, H2S,
галогены) или в жидких неэлектролитах (органические
жидкости – сернистая нефть).
ХИМИЧЕСКАЯ КОРРОЗИЯ В ГАЗОВОЙ СРЕДЕ
В общем виде для газовой коррозии:1.2Ме0 (т) + О2 (г) ⇄ 2 Ме+2О (т)
Образование оксида на поверхности металла в
результате взаимодействия с кислородом воздуха.
2. МеО (т) → [МеО] (р)
Растворение оксидной пленки в самом металле,
равновесие будет сдвинуто вправо, т.к. оксиды большинства
металлов способны растворяться в металле и уходить из
системы равновесия.
Механизм такой коррозии сводится к диффузии ионов
металла сквозь пленку продуктов коррозии с одной стороны,
и с другой стороны встречной диффузии атомов кислорода
вглубь пленки.
ПРИМЕР ХИМИЧЕСКОЙ КОРРОЗИИ В ЖИДКОЙ СРЕДЕ.
СКОРОСТЬ ОКИСЛЕНИЯ
Определяется свойствами оксидной пленки наповерхности металла:
сплошность пленки;
диффузионная способность пленки;
строение оксидной пленки.
Сплошность пленки () оценивается отношением объема
образовавшегося оксида к объему металла,
израсходованного на образование этого оксида (фактор
Пиллинга-Бэдвордса)
Значения для
металлов приведены в справочниках.
СПЛОШНОСТЬ ПЛЕНКИ
Если< 1, то образующаяся пленка не сплошная. Толщина
оксидной пленки растет пропорционально времени окисления.
С повышением температуры процесс коррозии резко
ускоряется из-за плохого отвода тепла, идет разогрев металла
и скорость реакции возрастает.
Если
= 1,2 – 1,6, то образующаяся оксидная пленка
сплошная. Такая пленка тормозит диффузию окислителя. И по
мере утолщения пленки ее дальнейший рост все время будет
замедляться. Сплошные пленки образуются на поверхности
таких металлов как Со, Ni, Mn, Ti.
При
> 1,6 оксидные пленки
также не сплошные и легко
отделяются
от
поверхности
металла (железная окалина)
ВОРОНЕНИЕ СТАЛИ
Воронеа́ниестали (оксидирование, чернение,
синение) -
процесс
получения
на
поверхности
углеродистой
или
низколегированной стали или чугуна слоя
окислов
железа толщиной 1-10 мкм. От толщины этого слоя зависит его
цвет - так называемые цвета побежалости, сменяющие друг
друга по мере роста плёнки (жёлтый, бурый, вишнёвый,
фиолетовый, синий, серый).
Структура покрытия мелкокристаллическая,
микропористая. Для придания блеска, а также
улучшения защитных свойств окисной плёнки
её также пропитывают маслом (минеральным
или растительным).
Сейчас воронение применяется
преимущественно в качестве декоративной
отделки, а раньше - в основном - для
уменьшения коррозии металла.
ВЛИЯНИЕ СТРОЕНИЯ ОКСИДНОЙ ПЛЕНКИ НА СКОРОСТЬ КОРРОЗИИ
Для металлов с переменной степенью окисления строениепленки по толщине будет различное, так, например, при
воронении стали образуются следующие оксидные слои:
Fe|диффузный слой|FeO|диффузный слой|Fe3O4
Такое строение оксидной пленки
обеспечивает прочную связь
оксидного слоя с поверхностью
металла.
Экспериментально доказано, что
оксидные пленки со структурой
шпинели RO.R2O3 (FeO.Cr2O3 или
NiO.Cr2O3) служат надежной
защитой от коррозии.
КОЛИЧЕСТВЕННАЯ ОЦЕНКА СКОРОСТИ КОРРОЗИИ
Количественно скорость любого вида коррозии измеряется вединицах массы потерянного металла (∆m) с единицы
площади (S) в единицу времени (t):
Скорость коррозии может измеряться и толщиной слоя
потерянного металла за единицу времени.
Для определения скорости коррозии используют весовые,
объемные и физические методы.
АГРЕССИВНЫЕ СРЕДЫ И УСТОЙЧИВОСТЬ РАЗЛИЧНЫХ МЕТАЛЛОВ
Кроме кислорода сильным агрессивным свойством обладаюти другие газы. Наиболее активными являются фтор (F),
диоксид серы (SO2), хлор (Cl2), сероводород (Н2S). Их
агрессивность по отношению к металлам, а следовательно и
скорость коррозий, не одинакова.
Например, алюминий и его сплавы,
хром и стали с высоким содержанием
хрома, неустойчивы в атмосфере,
содержащей
хлор,
хотя
по
отношению
к
кислороду
они
устойчивы.
Никель не устойчив в атмосфере
диоксида серы (SO2), а медь вполне
устойчива.
Электрохимическая коррозия металлов
ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
Электрохимическая коррозия характерна для сред, имеющихионную проводимость, т.е. для электролитов
В этом случае реакция взаимодействия металла с
окислителем протекает в несколько стадий:
1. Анодное
окисление
металла.
Металл в виде ионов переходит в
раствор,
а
эквивалентное
количество электронов остается в
_
металле: Me0 - ne → Меn+
2. Катодный процесс – ассимиляция
(удерживание)
избыточных
электронов в металле.
3. Движение ионов в растворе.
УСЛОВИЯ, СПОСОБСТВУЮЩИЕ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ
Положение металла в ряду активности металлов: чемдальше расположены друг от друга, тем быстрее
происходит коррозия.
Чистота металла: примеси ускоряют коррозию.
Неровности поверхности металла, трещины.
Грунтовые воды, морская вода, раствор электролита
(ионы: Н+, Сl-, Br-, I-, для амфотерных металлов ОН-).
Повышение температуры.
Действие
микроорганизмов
(грибов,
бактерий,
лишайников): воздействуют на металлы с высокой
коррозионной устойчивостью.
МЕХАНИЗМ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ. АНОДНЫЙ ПРОЦЕСС.
Механизмэлектрохимической
коррозии
определяется
разностью потенциалов катодных и анодных участков и
сводится к работе газового гальванического элемента.
Основным отличием процессов электрохимической коррозии
от процессов гальваническом элементе является отсутствие
внешней цепи. Электроны в этом случае не выходят из
корродирующего металла, а движутся внутри металла.
Так как, любой металл всегда содержит примеси других
металлов, то на его поверхности в среде электролита
образуется много короткозамкнутых микрогальванических
элементов.
Анодом в них будет основной металл, который окисляется по
_
реакции: Me0 - ne → Меn+
КАТОДНЫЙ ПРОЦЕСС ДЕПОЛЯРИЗАЦИИ.
Катодный процесс, чаще всего, идет с кислородной иливодородной деполяризацией.
Деполяризатор – это вещество удерживающее электроны.
Кислородная деполяризация происходит с участием
растворенного кислорода, который является
деполяризатором:
при
: О2 + 2Н2О + 4е- → 4ОНпри
: О2 + 2Н+ + 4е- → 2Н2О
Водородная деполяризация происходит с участием катионов
водорода среды (деполяризатор – водород):
при
: 2Н+ + 2е- → Н20
ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
Анод (-) Fe / О2, Н2О, NaCl / Sn (+) КатодA: Fe
0
_
- 2e → Fe
2+
_
СХЕМА КОРРОЗИОННОЙ МИКРОГАЛЬВАНОПАРЫ ПРИ КОНТАКТЕ Zn - Cu
Анод (-) Zn / среда / Сu (+) КатодАнод (-) Zn / О2, Н2О, NaCl / Сu (+) Катод
Zn
0
_
- 2e → Zn
2+
_
О2 + 2Н2О + 4е → 4ОНкислородная деполяризация
Анод (-) Zn / Н2SO4 / Сu (+) Катод
_
2Н+ + 2е → Н20
водородная деполяризация
СХЕМА МИКРОГАЛЬВАНОПАРЫ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ ПРИ КОНТАКТЕ ЖЕЛЕЗА ЦИНКА
Анод (-) Zn / О2, Н2О, NaCl / Fe (+) КатодАЭРАЦИОННАЯ КОРРОЗИЯ
Процессы окисления и восстановления идут на разныхучастках поверхности металла и сопровождаются появлением
электрического тока.
При неодинаковом доступе кислорода
к
поверхности
металла
на
ней
возникают
гальваническая
пара
особого
рода:
участок
более
адсорбирующий кислород является
катодом, а менее адсорбирующий
анодом.
Вследствие
сферической
сплющенности капли воды кольцевая
зона под ее краями окажется катодом,
а под центральной частью - анодом.
Анод (-) Fe (центр) / О2, Н2О, NaCl / Fe (край) (+) Катод
А: Fe2+ + K3 = 3K+ + Fe2+
гексацианоферрат (III) калия
«турнбулевая синь»
ПАССИВАЦИЯ МЕТАЛЛОВ ПРИ КОРРОЗИЯ
Иногда скорость коррозии может лимитироваться аноднымпроцессом. Это характерно для металлов, способных
пассивироваться (Cr, Al, Ti, Ni, Zr, Ta и др.)
Пассивность металла называется
состояние его повышенной
коррозионной устойчивости,
вызванное торможением
анодного процесса.
Пассивирование связано с образованием на поверхности
металла адсорбированных или фазовых слоев (иногда тех и
других), которые тормозят процесс растворения металла.
Сильные окислители обычно способствуют пассивированию
металла.
∆G = -nFE < 0
Е= Ϥ0Ох - Ϥ0Red > 0
Ϥ0Ох > Ϥ0Red
Ϥ0Ох > Ϥ0Me+n/Me0
УСЛОВИЯ ПРОТЕКАНИЯ КОРРОЗИИ С КИСЛОРОДНОЙ И ВОДОРОДНОЙ ДЕПОЛЯРИЗАЦИЕЙ
Если E0Me+n/Me0 < E0Н+/Н2 меньше потенциала водородногоэлектрода (область 1), возможна коррозия и с поглощением
кислорода, и с выделением водорода (щелочные и щелочноземельные металлы, цинк, алюминий)
Если E0Me+n/Me0 меньше потенциала кислородного электрода,
но больше потенциала водородного электрода (область 2),
тогда коррозия возможна только с участием кислорода.
_
E0Н+/Н2 < E0Me+n/Me0 < E0О2/ОН-
А (-): Ме0 - ne → Me+n
_
К (+): О2 + 2Н2О + 4е → 4ОН-
УСЛОВИЯ ПРОТЕКАНИЯ КОРРОЗИИ С КИСЛОРОДНОЙ И ВОДОРОДНОЙ ДЕПОЛЯРИЗАЦИЕЙ
Если E0Me+n/Me0 > E0О2/ОН- потенциала кислородного электрода(область 3), то коррозия металла невозможна.
Пример: золото – в отсутствии комплексообразователя не
корродирует с поглощением кислорода или выделением
водорода.
Потенциалы многих металлов лежат во второй области.
Методы защиты металлов от коррозии
МЕТОДЫ ЗАЩИТЫ МЕТАЛЛОВ ОТ КОРРОЗИИ
Все методы защиты условно делятся на следующие группы:1.Легирование металлов;
2.Защитные покрытия (металлические и неметаллические);
3.Электрохимическая защита;
4.Изменение свойств коррозионной среды.
Выбор того или иного способа защиты от коррозии
определяется:
с одной стороны его эффективностью,
с другой стороны его экономической целесообразностью.
ЛЕГИРОВАНИЕ МЕТАЛЛОВ
Это метод защиты, связанный сизменением свойств корродирующего
металла. Эффективный, хотя обычно
дорогой метод защиты. При
легировании в состав сплава обычно
вводят компоненты, вызывающие
пассивирование металла (введение
хрома, никеля, вольфрама и т.д.)
Для жаростойких сплавов легирующими
добавками являются хром, алюминий,
никель, кремний – они улучшают свойства
защитных пленок, образующихся при
окислении металлов.
ЗАЩИТНЫЕ ПОКРЫТИЯ. МЕТАЛЛИЧЕСКИЕ ПОКРЫТИЯ
Защитные покрытия - это слои, искусственно создаваемыена поверхности металла для предохранения от коррозии.
Металлические покрытия
Материалами для покрытия могут
быть как чистые металлы (Zn, Cd,
Al, Ni, Cu, Cr, Ag), так и их сплавы
(бронза, латунь).
По характеру поведения эти
покрытия делятся
на катодные и анодные
КАТОДНЫЕ МЕТАЛЛИЧЕСКИЕ ПОКРЫТИЯ
К катодным покрытиям относятся покрытия, электродныепотенциалы которых в данной среде имеют более
положительное значение, чем потенциал основного металла.
Для стали (Fe) катодным покрытием будет медное,
никелевое, серебренное.
Анод (-) Fe / О2, Н2О, NaCl / Сu (+) Катод
_
A: Fe 0 - 2e → Fe 2+
_
К: О2 + 2Н2О + 4е → 4ОН-
При повреждении катодного
покрытия возникает
кислородная деполяризация
гальванический элемент в
_
+
0
2Н + 2е → Н2
котором идет окисление
водородная деполяризация
основного материала.
Следовательно, катодное покрытие может защищать изделия
только при отсутствии пор и трещин, т.е. когда не нарушена
целостность покрытия.
АНОДНЫЕ МЕТАЛЛИЧЕСКИЕ ПОКРЫТИЯ
Анодные покрытия имеют более отрицательный потенциал,чем потенциал основного металла.
Например: покрытие
стали (Fe) цинком – основной металл в этом случае будет
катодом и корродировать не будет.
Анод (-) Zn / О2, Н2О, NaCl / Fe (+) Катод
_
A: Zn 0 - 2e → Zn 2+
_
К: О2 + 2Н2О + 4е → 4ОНкислородная деполяризация
_
2Н+ + 2е → Н20
водородная деполяризация
При
повреждении
анодного
покрытия
возникает
гальванический элемент в котором идет окисление
покрытия, а основной материал остается без изменения до
полного растворения покрытия.
СПОСОБЫ ПОЛУЧЕНИЯ МЕТАЛЛИЧЕСКИХ ЗАЩИТНЫХ ПОКРЫТИЙ
Электрохимический (гальванические покрытия).Металлизация (Погружение в расплавленный металл).
Термодиффузионный
способ
(для
получения
жаростойких покрытий: Al – алитирование, Si –
силицирование, Cr – хромирование, Ti - титанирование).
При повышенной температуре изделие погружают в
порошок
металла,
который
является
покрытием.
Происходит диффузия наносимого металла в основной
металл.
Химический.
Изделие
помещают
в
раствор,
содержащий ионы металла-покрытия и восстановитель. В
результате
окислительно-восстановительной
реакции
идет восстановление ионов металла до свободного
металла. Таким образом на металлы и неметаллы наносят
покрытия из серебра, меди, никеля и палладия.
НЕМЕТАЛЛИЧЕСКИЕ ПОКРЫТИЯ
Защитные свойства неметаллических покрытий сводится кизоляции металла от окружающей среды.
В качестве таких покрытий могут
быть:
неорганические эмали,
лакокрасочные покрытия,
покрытия смолами,
пластмассами,
полимернами пленками,
резиной.
ЭЛЕКТРОХИМИЧЕСКАЯ ЗАЩИТА. ПРОТЕКТОРЫ
Метод основан на торможении анодных или катодныхкоррозионных процессов.
Катодная защита – изделие подключается к (-) внешнего
источника тока, оно становится катодом, а анодом обычно
служит вспомогательный электрод (чаще всего стальной).
Если вспомогательный анод изготовлен из металла,
имеющего
более
отрицательный
потенциал,
чем
защищаемый металл, тогда ток не подключают. В
полученном гальваническом элементе растворяется анод, а
изделие не подвергается коррозии.
Такие электроды называются протекторами (магний и его
сплавы, цинк, алюминий).
Анодная защита – состоит в создании анодной поляризации
за счет приложенного извне тока (защита нержавеющий
стали в серной кислоте).
ИЗМЕНЕНИЕ СВОЙСТВ КОРРОЗИОННОЙ СРЕДЫ
Сцелью
снижения
коррозионной
активности
среды
проводят ее обработку.
Например:
удаление
кислорода
(кипячение
раствора;
барботаж инертным газом; восстановление его при помощи
соответствующих восстановителей – сульфиты, гидразин);
снижение концентрации ионов Н+
- подщелачиванием
раствора
В последние годы для защиты от коррозии широко
применяют ингибиторы.
ИНГИБИТОРЫ
Ингибитором – называется вещество, снижающее скоростькоррозии.
Ингибиторы используются в системах, работающих с
постоянным или малоизменяющимся объемом.
Наиболее четко ингибирующее действие выражено у
следующих типов соединений: амины, азотосодержащие
гетероциклические соединения, сульфиды, альдегиды,
меркаптаны.
По условиям применения ингибиторы делятся на:
ингибиторы для водных растворов (кислотные, щелочные
и для нейтральной сред);
«летучие ингибиторы» - для защиты от атмосферной
коррозии (соединения аминов с азотистой, угольной или
хромовой кислотами.)
МЕХАНИЗМ ДЕЙСТВИЯ ИНГИБИТОРОВ
Механизм действия ингибиторов заключается в адсорбцииих на корродирующей поверхности и последующем
торможении катодных и анодных процессов.
Анодные ингибиторы– окислители (NO2-, NO3-, CrO42-, PO43-).
Металл при этом переходит в устойчивое пассивное
состояние.
Катодные ингибиторы – снижают скорость катодного
процесса или сокращают площадь катодных участков.
Относятся органические вещества, содержащие серу, азот и
кислород (диэтиламин, уротропин, гидразин).
Материалы из металлов под химическим или электрохимическим воздействием окружающей среды подвергаются разрушению, которое называется коррозией. Коррозия металлов вызывается , в результате которых металлы переходят в окисленную форму и теряют свои свойства, что приводит в негодность металлические материалы.
Можно выделить 3 признака, характеризующих коррозию:
- Коррозия – это с химической точки зрения процесс окислительно-восстановительный.
- Коррозия – это самопроизвольный процесс, возникающий по причине неустойчивости термодинамической системы металл – компоненты окружающей среды.
- Коррозия – это процесс, который развивается в основном на поверхности металла. Однако, не исключено, что коррозия может проникнуть и вглубь металла.
Виды коррозии металлов
Наиболее часто встречаются следующие виды коррозии металлов :
- Равномерная – охватывает всю поверхность равномерно
- Неравномерная
- Избирательная
- Местная пятнами – корродируют отдельные участки поверхности
- Язвенная (или питтинг)
- Точечная
- Межкристаллитная – распространяется вдоль границ кристалла металла
- Растрескивающая
- Подповерхностная
С точки зрения механизма коррозионного процесса можно выделить два основных типа коррозии: химическую и электрохимическую.
Химическая коррозия металлов
Химическая коррозия металлов — это результат протекания таких химических реакций, в которых после разрушения металлической связи, атомы металла и атомы, входящие в состав окислителей, образуют . Электрический ток между отдельными участками поверхности металла в этом случае не возникает. Такой тип коррозии присущ средам, которые не способны проводить электрический ток – это газы, жидкие неэлектролиты.
Химическая коррозия металлов бывает газовой и жидкостной.
Газовая коррозия металлов – это результат действия агрессивных газовых или паровых сред на металл при высоких температурах, при отсутствии конденсации влаги на поверхности металла. Это, например, кислород, диоксид серы, сероводород, пары воды, галогены. Такая коррозия в одних случаях может привести к полному разрушению металла (если металл активный), а в других случаях на его поверхности может образоваться защитная пленка (например, алюминий, хром, цирконий).
Жидкостная коррозия металлов – может протекать в таких неэлектролитах, как нефть, смазочные масла, керосин и др. Этот тип коррозии при наличии даже небольшого количества влаги, может легко приобрести электрохимический характер.
При химической коррозии скорость разрушения металла пропорциональна и той скорости с которой окислитель проникает сквозь пленку оксида металла, покрывающую его поверхность. Оксидные пленки металлов могут проявлять или не проявлять защитные свойства, что определяется сплошностью.
Сплошность такой пленки оценивают величине фактора Пиллинга-Бэдвордса: (α = V ок /V Ме) по отношению объема образовавшегося оксида или другого какого-либо соединения к объему израсходованного на образование этого оксида металла
α = V ок /V Ме = М ок ·ρ Ме /(n·A Me ·ρ ок) ,
где V ок — объем образовавшегося оксида
V Ме — объем металла, израсходованный на образование оксида
М ок – молярная масса образовавшегося оксида
ρ Ме – плотность металла
n – число атомов металла
A Me — атомная масса металла
ρ ок — плотность образовавшегося оксида
Оксидные пленки, у которых α < 1 , не являются сплошными и сквозь них кислород легко проникает к поверхности металла. Такие пленки не защищают металл от коррозии. Они образуются при окислении кислородом щелочных и щелочно-земельных металлов (исключая бериллий).
Оксидные пленки, у которых 1 < α < 2,5 являются сплошными и способны защитить металл от коррозии.
При значениях α > 2,5 условие сплошности уже не соблюдается , вследствие чего такие пленки не защищают металл от разрушения.
Ниже представлены значения α для некоторых оксидов металлов
| металл | оксид | α | металл | оксид | α |
| K | K 2 O | 0,45 | Zn | ZnO | 1,55 |
| Na | Na 2 O | 0,55 | Ag | Ag 2 O | 1,58 |
| Li | Li 2 O | 0,59 | Zr | ZrO 2 | 1.60 |
| Ca | CaO | 0,63 | Ni | NiO | 1,65 |
| Sr | SrO | 0,66 | Be | BeO | 1,67 |
| Ba | BaO | 0,73 | Cu | Cu 2 O | 1,67 |
| Mg | MgO | 0,79 | Cu | CuO | 1,74 |
| Pb | PbO | 1,15 | Ti | Ti 2 O 3 | 1,76 |
| Cd | CdO | 1,21 | Cr | Cr 2 O 3 | 2,07 |
| Al | Al 2 O 2 | 1,28 | Fe | Fe 2 O 3 | 2,14 |
| Sn | SnO 2 | 1,33 | W | WO 3 | 3,35 |
| Ni | NiO | 1,52 |
Электрохимическая коррозия металлов
Электрохимическая коррозия металлов – это процесс разрушения металлов в среде различных , который сопровождается возникновением внутри системы электрического тока.
При таком типе коррозии атом удаляется из кристаллической решетки результате двух сопряженных процессов:
- Анодного – металл в виде ионов переходит в раствор.
- Катодного – образовавшиеся при анодном процессе электроны, связываются деполяризатором (вещество — окислитель).
Сам процесс отвода электронов с катодных участков называется деполяризацией, а вещества способствующие отводу – деполяризаторами.
Наибольшее распространение имеет коррозия металлов с водородной и кислородной деполяризацией .
Водородная деполяризация осуществляется на катоде при электрохимической коррозии в кислой среде
2H + +2e — = H 2 разряд водородных ионов
2H 3 O + +2e — = H 2 + 2H 2 O
Кислородная деполяризация осуществляется на катоде при электрохимической коррозии в нейтральной среде
O 2 + 4H + +4e — = H 2 O восстановление растворенного кислорода
O 2 + 2H 2 O + 4e — = 4OH —
Все металлы, по их отношению к электрохимической коррозии , можно разбить на 4 группы, которые определяются величинами их :
- Активные металлы (высокая термодинамическая нестабильность) – это все металлы, находящиеся в интервале щелочные металлы — кадмий (Е 0 = -0,4 В). Их коррозия возможна даже в нейтральных водных средах, в которых отсутствуют кислород или другие окислители.
- Металлы средней активности (термодинамическая нестабильность) – располагаются между кадмием и водородом (Е 0 = 0,0 В). В нейтральных средах, в отсутствии кислорода, не корродируют, но подвергаются коррозии в кислых средах.
- Малоактивные металлы (промежуточная термодинамическая стабильность) – находятся между водородом и родием (Е 0 = +0,8 В). Они устойчивы к коррозии в нейтральных и кислых средах, в которых отсутствует кислород или другие окислители.
- Благородные металлы (высокая термодинамическая стабильность) – золото, платина, иридий, палладий. Могут подвергаться коррозии лишь в кислых средах при наличии в них сильных окислителей.
Электрохимическая коррозия может протекать в различных средах. В зависимости от характера среды выделяют следующие виды электрохимической коррозии:
- Коррозия в растворах электролитов — в растворах кислот, оснований, солей, в природной воде.
- Атмосферная коррозия – в атмосферных условиях и в среде любого влажного газа. Это самый распространенный вид коррозии.
Например, при взаимодействии железа с компонентами окружающей среды, некоторые его участки служат анодом, где происходит окисление железа, а другие – катодом, где происходит восстановление кислорода:
А: Fe – 2e — = Fe 2+
K: O 2 + 4H + + 4e — = 2H 2 O
Катодом является та поверхность, где больше приток кислорода.
- Почвенная коррозия – в зависимости от состава почв, а также ее аэрации, коррозия может протекать более или менее интенсивно. Кислые почвы наиболее агрессивны, а песчаные – наименее.
- Аэрационная коррозия — возникает при неравномерном доступе воздуха к различным частям материала.
- Морская коррозия – протекает в морской воде, в связи с наличием в ней растворенных солей, газов и органических веществ.
- Биокоррозия – возникает в результате жизнедеятельности бактерий и других организмов, вырабатывающих такие газы как CO 2 , H 2 S и др., способствующие коррозии металла.
- Электрокоррозия – происходит под действием блуждающих токов на подземных сооружениях, в результате работ электрических железных дорог, трамвайных линий и других агрегатов.
Методы защиты от коррозии металла
Основной способ защиты от коррозии металла – это создание защитных покрытий – металлических, неметаллических или химических.
Металлические покрытия.
Металлическое покрытие наносится на металл, который нужно защитить от коррозии, слоем другого металла, устойчивого к коррозии в тех же условиях. Если металлическое покрытие изготовлено из металла с более отрицательным потенциалом (более активный) , чем защищаемый, то оно называется анодным покрытием . Если металлическое покрытие изготовлено из металла с более положительным потенциалом (менее активный), чем защищаемый, то оно называется катодным покрытием .
Например, при нанесении слоя цинка на железо, при нарушении целостности покрытия, цинк выступает в качестве анода и будет разрушаться, а железо защищено до тех пор, пока не израсходуется весь цинк. Цинковое покрытие является в данном случае анодным .
Катодным покрытием для защиты железа, может, например, быть медь или никель. При нарушении целостности такого покрытия, разрушается защищаемый металл.
Неметаллические покрытия.
Такие покрытия могут быть неорганические (цементный раствор, стекловидная масса) и органические (высокомолекулярные соединения, лаки, краски, битум).
Химические покрытия.
В этом случае защищаемый металл подвергают химической обработке с целью образования на поверхности пленки его соединения, устойчивой к коррозии. Сюда относятся:
оксидирование – получение устойчивых оксидных пленок (Al 2 O 3 , ZnO и др.);
фосфатирование – получение защитной пленки фосфатов (Fe 3 (PO 4) 2 , Mn 3 (PO 4) 2);
азотирование – поверхность металла (стали) насыщают азотом;
воронение стали – поверхность металла взаимодействует с органическими веществами;
цементация – получение на поверхности металла его соединения с углеродом.
Изменение состава технического металла также способствует повышению стойкости металла к коррозии. В этом случае в металл вводят такие соединения, которые увеличивают его коррозионную стойкость.
Изменение состава коррозионной среды (введение ингибиторов коррозии или удаление примесей из окружающей среды) тоже является средством защиты металла от коррозии.
Электрохимическая защита основывается на присоединении защищаемого сооружения катоду внешнего источника постоянного тока, в результате чего оно становится катодом. Анодом служит металлический лом, который разрушаясь, защищает сооружение от коррозии.
Протекторная защита – один из видов электрохимической защиты – заключается в следующем.
К защищаемому сооружению присоединяют пластины более активного металла, который называется протектором . Протектор – металл с более отрицательным потенциалом – является анодом, а защищаемое сооружение – катодом. Соединение протектора и защищаемого сооружения проводником тока, приводит к разрушению протектора.
Категории ,Company Logo Актуализация знаний и мотивация учебной деятельности Химический диктант по 2-м вариантам (нечётные номера – 1 вариант, чётные – 2 вариант) 1. Способность металлов хорошо проводить электрический ток объясняется наличием.. 2. Металлы имею … строение 3. От строения кристаллической решётки метал- ла зависят его… 4. Температура плавления металла зависит от… 5. Самый лёгкий металл… 6. Самый тяжёлый металл…
Company Logo Актуализация знаний и мотивация учебной деятельности 7.Металлы, плавящиеся при темп. ниже С называются… 8. Металлы с плотностью меньше 5 г/см 3 называются… 9. Темп. плавления тугоплавких металлов … 10. С повышением темп. плавления уменьшается… 11.Металлы, отдавая электроны, выполняют роль … 12. К чёрным металлам относятся…

Company Logo Актуализация знаний и мотивация учебной деятельности 13. Металлы в технике подразделяются по… 14. Самым тугоплавким металлом является… Мотивация: в древности людям было известно 7 металлов. Их число соотносилось Числу известных тогда планет: Сатурн-свинец, Меркурий-ртуть, Марс-железо, Луна-серебро, Солнце-золото, Венера-медь, Юпитер-олово. Вы знаете намного больше алхимиков и мы сегодня продолжим изучать свойства металлов

Company Logo Металлы 1. Что объединяет эти элементы? 2. Какие свойства этих элементов вам известны?

Company Logo Химические свойства металлов Какие свойства простых веществ изображены на этом слайде?

Company Logo Химические свойства металлов Какие элементы относятся к металлам? Назовите основное свойство металлов Как изменяется активность металлов в периоде? Элементы, на внешнем уровне у которых 1-2 электрона. Основное свойство - отдавать валентные электроны С увеличением заряда ядра активность металла в периоде уменьшается

Company Logo Ряд активности металлов Увеличение восстановительных свойств Рассмотрите ряд активности металлов, сделайте вывод об активности различных металлов, выскажите предположение с какими веществами они могут реагировать.

Company Logo Химические свойства металлов Взаимодействие с неметаллами: с кислородом с серой с галогенами Li K Ca Na Mg Al Zn Cr Fe Ni Pb Cu Hg Ag Pt Au При обычных условиях M + О2 оксид Медленно или при нагревании M + O 2 оксид M + O 2

Company Logo Химические свойства металлов Напишите уравнения реакций взаимодействия натрия с: кислородом, серой, хлором 4Na + O2 = 2Na2O 2Na + S = Na2S 2 Na + CI2 = 2NaCI

Company Logo Взаимодействие со сложными веществами: с водой Li K Ca NaMg Al Zn Cr Fe Ni Pb (H 2) Cu Hg Ag Pt Au При обычных условиях M + H 2 O H 2 + щёлочь При нагревании M+H 2 OH 2 +оксид M + H 2 O

Company Logo Примеры Закончите возможные уравнения реакций: 1. Li + H2O = 2. AI + H2O = 3. Hg + H2O = 2Li + 2HOH = 2LiOH + H2 2AI +3H2O = Ai2O3 + 3H2 Hg + H2O

Company Logo Взаимодействие с растворами кислот Li K Ca Na Mg Al |Zn Cr Fe Ni Pb (H 2) Cu Hg Ag Pt Au Вытесняют H 2 из растворов кислот Не вытесняют H 2 из растворов кислот

Company Logo Примеры Напишите возможные уравнения реакций взаимодействия с разбавленной серной кислотой: алюминия, цинка, натрия и меди 3H2SO4 + 2AI= AI2(SO4)3+ 3H2 H2SO4 + Zn = ZnSO4 + H2 H2SO4 + 2Na = Na2SO4 + H2 H2SO4 + Cu

Company Logo Взаимодействие с растворами солей Каждый металл вытесняет из растворов солей другие металлы, находящиеся правее него в ряду напряжений, и сам может быть вытеснен металлами, расположенными левее. Fe + CuSO4 = FeSO4 + Cu Zn + NiCI2 = ZnCI2 + Ni Запомнить! Нельзя для этой цели брать активные металлы, так как они взаимодействую с водой, образуя щёлочи.

Company Logo Реагирующи е вещества KCaFeCuAu О2 Н2О HCl (раствор) Pb(NO3)2 раствор Упражнения

Company Logo Проверка Реагирующие вещества NaCaFeCuAu О2О Н2ОН2О HCl (раствор) Pb(NO 3) 2 раствор +++--

Company Logo Коррозия Коррозия – это самопроизвольный процесс разрушения материалов и изделий из них под химическим воздействием окружающей среды.

Company Logo Причины коррозии А) газы (O2,SO2, H2S, Cl2, NH3, NO, NO2, H2O-пар и т.д.); сажа – адсорбент газов; Б) электролиты: щёлочи, кислоты, соли; В) ионы Сl-, влажность воздуха; Г) макро- и микроорганизмы; Е) блуждающий электрический ток; Ж) разнородность металлов.

Company Logo Виды коррозии Коррозия Атмосферная Газовая Химическая Электрохимическая

Company Logo Атмосферная Атмосферная коррозия металлов происходит во влажном воздухе при обычной температуре

Company Logo Химическая коррозия Химическая коррозия – это химическое разрушение металлов под действием кислорода, сероводорода и других газов в отсутствие влаги

Company Logo Газовая коррозия Газовая коррозия разновидность химической коррозии, которой поддается арматура печей, детали двигателей, которые работают в условиях высоких температур.

Company Logo Электрохимическая коррозия Электрохимическая коррозия – это разрушение металла, который находится в контакте с другим металлом и электролитом или водой.

Company Logo Электрохимическая коррозия На поверхности любого металла конденсируется вода, в которой растворены атмосферные газы, то есть образуется электролит. Если металл содержит примеси или соприкасается с другим металлом, начинается электрохимическая коррозия. При этом первым разрушается более активный металл

Company Logo Последствия коррозии Ежегодно прямые потери от ржавчины из-за некачественной защиты аппаратуры, оборудования и конструкций составляют порядка 10% от всего объема металла, производимого в мире.

Company Logo Защита металлов от коррозии Защитные покрытия- нанесение защитных покрытий на поверхность металла Легирующие добавки- добавление хрома,никеля, титана,кобальта Ингибиторы- добавление катализаторов,замедляющих химические реакции Протекторная защита – создание контакта с более активным металлом

Company Logo Закрепление полученных знаний Что называется коррозией? Какие факторы её вызывают? Разрушение металлов и сплавов под действием различных внешних факторов. Влияние атмосферного воздуха, грунтовой влаги, агрессивных газов Агрессивная химическая среда Электролиты

Company Logo Закрепление полученных знаний Назовите виды коррозии. Назовите способы защиты металлов от коррозии Атмосферная, химическая, газовая и электрохимическая. Защитные покрытия, легирующие добавки, ингибиторы протекторная защита

Элементы с металлическими свойствами расположены вIA – VIA группах Периодической системы (табл. 7).
Металлами являются также все элементы, расположенные вIБ – VIIIБ ‑группах (переходные металлы).
В настоящее время в Периодической системе 92 металла.
Типичными металлами являются s‑элементы (элементы IA‑группы от Li до Fr, элементы IIA‑группы от Mg до Ra). Общая электронная формула их атомов ns 1–2 . Для них характерны степени окисления +I и +II соответственно.
Небольшое число электронов (1–2) на внешнем энергетическом уровне атомов типичных металлов предполагает легкую потерю этих электронов и проявление сильных восстановительных свойств, что отражают низкие значения электроотрицательности. Отсюда вытекает ограниченность химических свойств и способов получения типичных металлов.
Характерной особенностью типичных металлов является стремление их атомов образовывать катионы и ионные химические связи с атомами неметаллов. Соединения типичных металлов с неметаллами – это ионные кристаллы «катион металлаанион неметалла», например К + Br ‑ , Са 2+ O 2‑ . Катионы типичных металлов входят также в состав соединений со сложными анионами – гидроксидов и солей, например Mg 2+ (OH ‑) 2 , (Li +) 2 CO 3 2‑ .
Металлы А‑групп, образующие диагональ амфотерности в Периодической системе Be‑Al‑Ge‑Sb‑Po, а также примыкающие к ним металлы (Ga, In, Tl, Sn, Pb, Bi) не проявляют типично металлических свойств. Общая электронная формула их атомов ns 2 np 0–4 предполагает большее разнообразие степеней окисления, большую способность удерживать собственные электроны, постепенное понижение их восстановительной способности и появление окислительной способности, особенно в высоких степенях окисления (характерные примеры – соединения Тl III , Pb IV , Bi v). Подобное химическое поведение характерно и для большинства d‑элементов, т. е. элементов Б‑групп Периодической системы (типичные примеры – амфотерные элементы Cr и Zn).
Это проявление двойственности (амфотерности) свойств, одновременно металлических (основных) и неметаллических, обусловлено характером химической связи. В твердом состоянии соединения нетипичных металлов с неметаллами содержат преимущественно ковалентные связи (но менее прочные, чем связи между неметаллами). В растворе эти связи легко разрываются, а соединения диссоциируют на ионы (полностью или частично). Например, металл галлий состоит из молекул Ga 2 , в твердом состоянии хлориды алюминия и ртути(II) AlCl 3 и HgCl 2 содержат сильно ковалентные связи, но в растворе AlCl 3 диссоциирует почти полностью, a HgCl 2 – в очень малой степени (да и то на ионы HgCl + и Cl ‑).
В свободном виде все металлы – твердые вещества, кроме одного – ртути Hg, которая при обычных условиях жидкость. В кристаллах металлов преобладает особый вид связи (металлическая связь); валентные электроны слабо связаны с конкретным атомом в решетке, и внутри металла существует так называемый электронный газ. Все металлы обладают высокой электропроводимостью (наибольшая y Ag, Cu, Аи, Al, Mg) и теплопроводностью. Встречаются низкоплавкие металлы (цезий Cs с температурой плавления 28,7 °C плавится от тепла руки) и, наоборот, весьма тугоплавкие (вольфрам W плавится лишь при 3387 °C). Отличительным свойством металлов служит их пластичность (ковкость), вследствие чего они могут быть прокатаны в тонкие листы – фольгу (Sn, Al, Au) или вытянуты в проволоку (Cu, Al, Fe), однако встречаются и очень хрупкие металлы (Zn, Sb, Bi).
В промышленности часто используют не чистые металлы, а их смеси – сплавы, в которых полезные свойства одного металла дополняются полезными свойствами другого. Так, медь обладает невысокой твердостью и малопригодна для изготовления деталей машин, сплавы же меди с цинком (латунь ) являются уже достаточно твердыми и широко используются в машиностроении. Алюминий обладает высокой пластичностью и достаточной легкостью (малой плотностью), но слишком мягок. На его основе готовят сплав с магнием, медью и марганцем – дуралюмин (дюраль), который, не теряя полезных свойств алюминия, приобретает высокую твердость и становится пригодным в авиастроении. Сплавы железа с углеродом (и добавками других металлов) – это широко известные чугун и сталь.
Металлы в свободном виде являются восстановителями . Однако реакционная способность некоторых металлов невелика из‑за того, что они покрыты поверхностной оксидной пленкой, в разной степени устойчивой к действию таких химических реактивов, как вода, растворы кислот и щелочей.
Например, свинец всегда покрыт оксидной пленкой, для его перехода в раствор требуется не только воздействие реактива (например, разбавленной азотной кислоты), но и нагревание. Оксидная пленка на алюминии препятствует его реакции с водой, но под действием кислот и щелочей разрушается. Рыхлая оксидная пленка {ржавчина ), образующаяся на поверхности железа во влажном воздухе, не мешает дальнейшему окислению железа.
Под действием концентрированных кислот на металлах образуется устойчивая оксидная пленка. Это явление называется пассивацией. Так, в концентрированной серной кислоте пассивируются (и после этого не реагируют с кислотой) такие металлы, как Be, Bi, Со, Fe, Mg и Nb, а в концентрированной азотной кислоте – металлы Al, Be, Bi, Со, Cr, Fe, Nb, Ni, Pb, Th и U.
При взаимодействии с окислителями в кислых растворах большинство металлов переходит в катионы, заряд которых определяется устойчивой степенью окисления данного элемента в соединениях (Na + , Са 2+ , Al 3+ , Fe 2+ и Fe 3+).
Восстановительная активность металлов в кислом растворе передается рядом напряжений. Большинство металлов переводится в раствор соляной и разбавленной серной кислотами, но Cu, Ag и Hg – только серной (концентрированной) и азотной кислотами, a Pt и Аи – «царской водкой».
Нежелательным химическим свойством металлов является их коррозия, т. е. активное разрушение (окисление) при контакте с водой и под воздействием растворенного в ней кислорода (кислородная коррозия). Например, широко известна коррозия железных изделий в воде, в результате чего образуется ржавчина, и изделия рассыпаются в порошок.
Коррозия металлов протекает в воде также из‑за присутствия растворенных газов СO 2 и SO 2 ; создается кислотная среда, и катионы Н + вытесняются активными металлами в виде водорода Н 2 (водородная коррозия).
Особенно коррозионно‑опасным может быть место контакта двух разнородных металлов (контактная коррозия). Между одним металлом, например Fe, и другим металлом, например Sn или Cu, помещенными в воду, возникает гальваническая пара. Поток электронов идет от более активного металла, стоящего левее в ряду напряжений (Fe), к менее активному металлу (Sn, Cu), и более активный металл разрушается (корродирует).
Именно из‑за этого ржавеет луженая поверхность консервных банок (железо, покрытое оловом) при хранении во влажной атмосфере и небрежном обращении с ними (железо быстро разрушается после появления хотя бы небольшой царапины, допускающей контакт железа с влагой). Напротив, оцинкованная поверхность железного ведра долго не ржавеет, поскольку даже при наличии царапин корродирует не железо, а цинк (более активный металл, чем железо).
Сопротивление коррозии для данного металла усиливается при его покрытии более активным металлом или при их сплавлении; так, покрытие железа хромом или изготовление сплава железа с хромом устраняет коррозию железа. Хромированное железо и сталь, содержащая хром (нержавеющая сталь), имеют высокую коррозионную стойкость.
Общие способы получения металлов в промышленности:
электрометаллургия, т. е. получение металлов электролизом расплавов (для наиболее активных металлов) или растворов солей;
пирометаллургия, т. е. восстановление металлов из руд при высокой температуре (например, получение железа в доменном процессе);
гидрометаллургия, т. е. выделение металлов из растворов их солей более активными металлами (например, получение меди из раствора CuSO 4 действием цинка, железа или алюминия).
В природе иногда встречаются самородные металлы (характерные примеры – Ag, Au, Pt, Hg), но чаще металлы находятся в виде соединений (металлические руды). По распространенности в земной коре металлы различны: от наиболее распространенных – Al, Na, Са, Fe, Mg, К, Ti до самых редких – Bi, In, Ag, Au, Pt, Re.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Все темы данного раздела:
Распространенные элементы. строение атомов. Электронные оболочки. Орбитали
Химический элемент – определенный вид атомов, обозначаемый названием и символом и характеризуемый порядковым номером и относительной атомной массой.
В табл. 1 перечи
В каждой орбитали может разместиться не более двух электронов
Один электрон на орбитали называется неспаренным, два электрона – электронной парой:
Свойства элементов находятся в периодической зависимости от порядкового номера
Периодически повторяющийся характер изменения состава электронной оболочки атомов элементов объясняет периодическое изменение свойств элементов при движении по периодам и группам Пе
Молекулы. Химическая связь. Строение веществ
Химические частицы, образованные из двух или нескольких атомов, называются молекулами (реальными или условными формульными единицами многоатомных веществ). Атомы в мол
Кальций
Кальций – элемент 4‑го периода и IIA‑группы Периодической системы, порядковый номер 2O. Электронная формула атома 4s2, степени окислен
Алюминий
Алюминий – элемент 3‑го периода и IIIA‑группы Периодической системы, порядковый номер 13. Электронная формула атома 3s23p1,
Марганец
Марганец – элемент 4‑го периода и VIIB‑группы Периодической системы, порядковый номер 25. Электронная формула атома 3d54s2;
Водород
Водород – первый элемент Периодической системы (1‑й период, порядковый номер 1). Не имеет полной аналогии с остальными химическими элементами и не принадлежит ни к како
Хлор. Хлороводород
Хлор – элемент 3‑го периода и VII А‑группы Периодической системы, порядковый номер 17. Электронная формула атома 3s23p5, ха
Хлориды
Хлорид натрия NaCl. Бескислородная соль. Бытовое название поваренная соль. Белый, слабогигроскопичный. Плавится и кипит без разложения. Умеренно раствори
Гипохлориты. Хлораты
Гипохлорит кальция Са(СlO)2. Соль хлорноватистой кислоты HClO. Белый, при нагревании разлагается без плавления. Хорошо растворим в холодной воде (обр
Бромиды. Иодиды
Бромид калия КBr. Бескислородная соль. Белый, негигроскопичный, плавится без разложения. Хорошо растворим в воде, гидролиза нет. Восстановитель (более слабый, ч
Кислород
Кислород – элемент 2‑го периода и VIA‑группы Периодической системы, порядковый номер 8, относится к халькогенам (но чаще рассматривается отдельно). Электронная фо
Сера. Сероводород. Сульфиды
Сера – элемент 3‑го периода и VIA‑группы Периодической системы, порядковый номер 16, относится к халькогенам. Электронная формула атома 3s
Диоксид серы. Сульфиты
Диоксид серы SO2. Кислотный оксид. Бесцветный газ с резким запахом. Молекула имеет строение незавершенного треугольника [: S(O)2] (sр
Серная кислота. Сульфаты
Серная кислота H2SO4. Оксокислота. Бесцветная жидкость, очень вязкая (маслообразная), весьма гигроскопичная. Молек
Азот. Аммиак
Азот – элемент 2‑го периода и VA‑группы Периодической системы, порядковый номер 7. Электронная формула атома 2s22p3, характе
Оксиды азота. Азотная кислота
Монооксид азота NO. Несолеобразующий оксид. Бесцветный газ. Радикал, содержит ковалентную σπ‑связь (N=O), в твердом состоянии димер N2
Нитриты. Нитраты
Нитрит калияKNO2. Оксосоль. Белый, гигроскопичный. Плавится без разложения. Устойчив в сухом воздухе. Очень хорошо растворим в воде (образуется бесцв
Углерод в свободном виде
Углерод – элемент 2‑го периода и IVA‑группы Периодической системы, порядковый номер 6. Химия углерода – это в основном химия органических соединений; неорганическ
Оксиды углерода
Монооксид углерода СО. Несолеобразующий оксид. Бесцветный газ, без запаха, легче воздуха. Молекула слабополярна, содержит ковалентную тройную σππ
Карбонаты
Карбонат натрия Na2CO3. Оксосоль. Техническое название кальцинированная сода. Белый, при нагревании плавится и разлагается. Чувстви
Кремний
Кремний – элемент 3‑го периода и IVA‑группы Периодической системы, порядковый номер 14. Электронная формула атома 3s23p2. Х
Алканы. Циклоалканы
Алканы (парафины) – это соединения углерода с водородом, в молекулах которых атомы углерода соединены между собой одинарной связью (предельные углеводоро
Алкены. Алкадиены
Алкены (олефины) – это углеводороды, в молекулах которых содержатся атомы углерода, соединенные между собой двойной связью (непредельные углеводороды ряд
Спирты. Простые эфиры. Фенолы
Спирты – производные углеводородов, содержащие функциональную группу ОН (гидроксил). Спирты, в которых имеется одна группа ОН, называются одноат
Альдегиды и кетоны
Альдегиды и кетоны – это производные углеводородов, содержащие функциональную карбонильную группу СО. В альдегидах карбонильная группа связана с а
Карбоновые кислоты. Сложные эфиры. Жиры
Карбоновые кислоты – это производные углеводородов, содержащие функциональную группу СООН (карбоксил).
Формулы и названия некоторых распространенных ка
Углеводы
Углеводы (сахара) – важнейшие природные соединения, состоящие из углерода, водорода и кислорода. Углеводы подразделяются на моносахариды, дисахариды и полис
Нитросоединения. Амины
Очень важны в народном хозяйстве азотсодержащие органические вещества. Азот может входить в органические соединения в виде нитрогруппы NO2, аминогруппы NH2 и а
Аминокислоты. Белки
Аминокислоты – органические соединения, содержащие в своем составе две функциональные группы – кислотную СООН и аминную NH2
Скорость реакций
Количественной характеристикой быстроты течения химической реакции А + B → D + E является ее скорость, т. е. скорость взаимодействия частиц реагентов А
Скорость химической реакции прямо пропорциональна произведению молярных концентраций реагентов
если для реакции необходимо столкновение двух реагирующих молекул. Эта зависимость носит название кинетического закона действующих масс (К. Гулльберг, П. Вог
Энергетика реакций
Любая реакция сопровождается выделением или поглощением энергии в форме теплоты. В исходных веществах химические связи разрываются, и на это энергия затрачивается (т. е. она при это
Обратимость реакций
Химическая реакция называется обратимой, если в данных условиях протекает не только прямая реакция (→), но также и обратная реакция т. е. из исходных веществ образуются
При воздействии на равновесную систему химическое равновесие смещается в сторону, противодействующую этому воздействию
Рассмотрим подробнее влияние таких факторов, как температура, давление, концентрация, на смещение равновесия.
1. Температура. Повышение температуры сме
Растворимость веществ в воде
Раствор – это гомогенная система, состоящая из двух или более веществ, содержание которых можно изменять в определенных пределах без нарушения однородности.
Электролитическая диссоциация
Растворение любого вещества в воде сопровождается образованием гидратов. Если при этом в растворе не происходит формульных изменений у частиц растворенного вещества, то такие вещест
Диссоциация воды. Среда растворов
Сама вода – это очень слабый электролит:
Реакции ионного обмена
В разбавленных растворах электролитов (кислот, оснований, солей) химические реакции протекают обычно при участии ионов. При этом все элементы реагентов могут сохра
Гидролиз солей
Гидролиз соли – это взаимодействие ее ионов с водой, приводящее к появлению кислотной или щелочной среды, но не сопровождающееся образованием осадка или газа (ниже
Окислители и восстановители
Окислительно‑восстановительные реакции протекают с одновременным повышением и понижением степеней окисления элементов и сопровождаются передачей электронов:
Подбор коэффициентов методом электронного баланса
Метод состоит из нескольких этапов.
1. Записывают схему реакции; находят элементы, повышающие и понижающие свои степени окисления, и выпи
Ряд напряжений металлов
В ряду напряжений металлов стрелка отвечает уменьшению восстановительной способности металлов и увеличению окислительной способности их катионов в водном растворе (кислотная среда):
Электролиз расплава и раствора
Электролизом называется окислительно‑восстановительный процесс, протекающий на электродах при прохождении постоянного электрического тока через растворы или
Массовая доля растворенного вещества. Разбавление, концентрирование и смешивание растворов
Массовая доля растворенного вещества В
(ω в) – это отношение массы вещества В (т в) к массе раствора (m (р)
Объемное отношение газов
Для химической реакции a A + b B = c C + d D выполняется соотношение
Масса (объем, количество вещества) продукта по реагенту в избытке или с примесями
Избыток и недостаток реагентов. Количества, массы и объемы (для газов) реагентов не всегда берутся стехиометрическими, т. е. в соответствии с уравнениями реакции. Ч
Нахождение молекулярной формулы органического соединения
При выведении формул веществ, особенно в органической химии, часто используют относительную плотность газа.
Относительная плотность газа X – отношение абсолютной пло
Элементы с металлическими свойствами расположены вIA – VIA группах Периодической системы (табл. 7).
Металлами являются также все элементы, расположенные вIБ – VIIIБ ‑группах (переходные металлы).
В настоящее время в Периодической системе 92 металла.
Типичными металлами являются s‑элементы (элементы IA‑группы от Li до Fr, элементы IIA‑группы от Mg до Ra). Общая электронная формула их атомов ns 1–2 . Для них характерны степени окисления +I и +II соответственно.
Небольшое число электронов (1–2) на внешнем энергетическом уровне атомов типичных металлов предполагает легкую потерю этих электронов и проявление сильных восстановительных свойств, что отражают низкие значения электроотрицательности. Отсюда вытекает ограниченность химических свойств и способов получения типичных металлов.
Характерной особенностью типичных металлов является стремление их атомов образовывать катионы и ионные химические связи с атомами неметаллов. Соединения типичных металлов с неметаллами – это ионные кристаллы «катион металлаанион неметалла», например К + Br ‑ , Са 2+ O 2‑ . Катионы типичных металлов входят также в состав соединений со сложными анионами – гидроксидов и солей, например Mg 2+ (OH ‑) 2 , (Li +) 2 CO 3 2‑ .
Металлы А‑групп, образующие диагональ амфотерности в Периодической системе Be‑Al‑Ge‑Sb‑Po, а также примыкающие к ним металлы (Ga, In, Tl, Sn, Pb, Bi) не проявляют типично металлических свойств. Общая электронная формула их атомов ns 2 np 0–4 предполагает большее разнообразие степеней окисления, большую способность удерживать собственные электроны, постепенное понижение их восстановительной способности и появление окислительной способности, особенно в высоких степенях окисления (характерные примеры – соединения Тl III , Pb IV , Bi v). Подобное химическое поведение характерно и для большинства d‑элементов, т. е. элементов Б‑групп Периодической системы (типичные примеры – амфотерные элементы Cr и Zn).
Это проявление двойственности (амфотерности) свойств, одновременно металлических (основных) и неметаллических, обусловлено характером химической связи. В твердом состоянии соединения нетипичных металлов с неметаллами содержат преимущественно ковалентные связи (но менее прочные, чем связи между неметаллами). В растворе эти связи легко разрываются, а соединения диссоциируют на ионы (полностью или частично). Например, металл галлий состоит из молекул Ga 2 , в твердом состоянии хлориды алюминия и ртути(II) AlCl 3 и HgCl 2 содержат сильно ковалентные связи, но в растворе AlCl 3 диссоциирует почти полностью, a HgCl 2 – в очень малой степени (да и то на ионы HgCl + и Cl ‑).
В свободном виде все металлы – твердые вещества, кроме одного – ртути Hg, которая при обычных условиях жидкость. В кристаллах металлов преобладает особый вид связи (металлическая связь); валентные электроны слабо связаны с конкретным атомом в решетке, и внутри металла существует так называемый электронный газ. Все металлы обладают высокой электропроводимостью (наибольшая y Ag, Cu, Аи, Al, Mg) и теплопроводностью. Встречаются низкоплавкие металлы (цезий Cs с температурой плавления 28,7 °C плавится от тепла руки) и, наоборот, весьма тугоплавкие (вольфрам W плавится лишь при 3387 °C). Отличительным свойством металлов служит их пластичность (ковкость), вследствие чего они могут быть прокатаны в тонкие листы – фольгу (Sn, Al, Au) или вытянуты в проволоку (Cu, Al, Fe), однако встречаются и очень хрупкие металлы (Zn, Sb, Bi).
В промышленности часто используют не чистые металлы, а их смеси – сплавы, в которых полезные свойства одного металла дополняются полезными свойствами другого. Так, медь обладает невысокой твердостью и малопригодна для изготовления деталей машин, сплавы же меди с цинком (латунь ) являются уже достаточно твердыми и широко используются в машиностроении. Алюминий обладает высокой пластичностью и достаточной легкостью (малой плотностью), но слишком мягок. На его основе готовят сплав с магнием, медью и марганцем – дуралюмин (дюраль), который, не теряя полезных свойств алюминия, приобретает высокую твердость и становится пригодным в авиастроении. Сплавы железа с углеродом (и добавками других металлов) – это широко известные чугун и сталь.
Металлы в свободном виде являются восстановителями . Однако реакционная способность некоторых металлов невелика из‑за того, что они покрыты поверхностной оксидной пленкой, в разной степени устойчивой к действию таких химических реактивов, как вода, растворы кислот и щелочей.
Например, свинец всегда покрыт оксидной пленкой, для его перехода в раствор требуется не только воздействие реактива (например, разбавленной азотной кислоты), но и нагревание. Оксидная пленка на алюминии препятствует его реакции с водой, но под действием кислот и щелочей разрушается. Рыхлая оксидная пленка {ржавчина ), образующаяся на поверхности железа во влажном воздухе, не мешает дальнейшему окислению железа.
Под действием концентрированных кислот на металлах образуется устойчивая оксидная пленка. Это явление называется пассивацией. Так, в концентрированной серной кислоте пассивируются (и после этого не реагируют с кислотой) такие металлы, как Be, Bi, Со, Fe, Mg и Nb, а в концентрированной азотной кислоте – металлы Al, Be, Bi, Со, Cr, Fe, Nb, Ni, Pb, Th и U.
При взаимодействии с окислителями в кислых растворах большинство металлов переходит в катионы, заряд которых определяется устойчивой степенью окисления данного элемента в соединениях (Na + , Са 2+ , Al 3+ , Fe 2+ и Fe 3+).
Восстановительная активность металлов в кислом растворе передается рядом напряжений. Большинство металлов переводится в раствор соляной и разбавленной серной кислотами, но Cu, Ag и Hg – только серной (концентрированной) и азотной кислотами, a Pt и Аи – «царской водкой».
Нежелательным химическим свойством металлов является их коррозия, т. е. активное разрушение (окисление) при контакте с водой и под воздействием растворенного в ней кислорода (кислородная коррозия). Например, широко известна коррозия железных изделий в воде, в результате чего образуется ржавчина, и изделия рассыпаются в порошок.
Коррозия металлов протекает в воде также из‑за присутствия растворенных газов СO 2 и SO 2 ; создается кислотная среда, и катионы Н + вытесняются активными металлами в виде водорода Н 2 (водородная коррозия).
Особенно коррозионно‑опасным может быть место контакта двух разнородных металлов (контактная коррозия). Между одним металлом, например Fe, и другим металлом, например Sn или Cu, помещенными в воду, возникает гальваническая пара. Поток электронов идет от более активного металла, стоящего левее в ряду напряжений (Fe), к менее активному металлу (Sn, Cu), и более активный металл разрушается (корродирует).
Именно из‑за этого ржавеет луженая поверхность консервных банок (железо, покрытое оловом) при хранении во влажной атмосфере и небрежном обращении с ними (железо быстро разрушается после появления хотя бы небольшой царапины, допускающей контакт железа с влагой). Напротив, оцинкованная поверхность железного ведра долго не ржавеет, поскольку даже при наличии царапин корродирует не железо, а цинк (более активный металл, чем железо).
Сопротивление коррозии для данного металла усиливается при его покрытии более активным металлом или при их сплавлении; так, покрытие железа хромом или изготовление сплава железа с хромом устраняет коррозию железа. Хромированное железо и сталь, содержащая хром (нержавеющая сталь), имеют высокую коррозионную стойкость.
Общие способы получения металлов в промышленности:
электрометаллургия, т. е. получение металлов электролизом расплавов (для наиболее активных металлов) или растворов солей;
пирометаллургия, т. е. восстановление металлов из руд при высокой температуре (например, получение железа в доменном процессе);
гидрометаллургия, т. е. выделение металлов из растворов их солей более активными металлами (например, получение меди из раствора CuSO 4 действием цинка, железа или алюминия).
В природе иногда встречаются самородные металлы (характерные примеры – Ag, Au, Pt, Hg), но чаще металлы находятся в виде соединений (металлические руды). По распространенности в земной коре металлы различны: от наиболее распространенных – Al, Na, Са, Fe, Mg, К, Ti до самых редких – Bi, In, Ag, Au, Pt, Re.
Примеры заданий части A
1. В железосодержащих продуктах реакций между железом и разбавленными кислотами HCl, H 2 SO 4 и HNO 3 общая сумма числа атомов всех элементов равна
2. В уравнениях реакций
Fe + O 2 → (Fe II Fe III 2)O 4
Fe + Cl 2 → FeCl 3
Fe + Н 2 O (пар) → (Fe II Fe III 2)O 4 + Н 2
3. Соль NaCrO 2 получают при взаимодействии между
1) CrO 3 и Na 2 O
2) Cr 2 O 3 и Na 2 CO 3
4) CrO 2 и NaHCO 3
4. Будет протекать реакция при внесении меди в разбавленные растворы
1) бромоводорода
2) нитрата ртути(II)
3) серной кислоты
4) азотной кислоты
5. Протекают реакции
1) H 2 SO 4 + FeCO 3 →…
2) AgNO 3 + HI (p‑p) →…
3) K 2 Cr 2 O 7 (p‑p) + PbO 2 →…
4) AgNOg (p‑p) + Au →…
6–9. Масса тигля из
6. платины
8. серебра
при прокаливании на воздухе
1) уменьшается
2) увеличивается
3) не изменяется
4) не знаю
10–11. В молекулярных уравнениях реакций
10. Fe 2 O 3 + HNOg →…, Fe(OH) 2 + O 2 → FeO(OH) +…
11. CuO + С → CO 2 + Cu, Fe 2 O 3 + CO → Fe +…
общая сумма коэффициентов равна
12. Сплав, оба компонента которого реагируют с концентрированной азотной кислотой, – это
13. He протекает реакция замещения между реагентами
2) Pb(NO 3) 2 и Cr
4) Cd и Hg(NO 3) 2
14. Для удаления примеси NiSO 4 из раствора FeSO 4 надо добавить
1) хлорид бария
2) нитрат серебра(I)
3) гидроксид калия
15. Пластинка металла окажется покрытой другим металлом, взятым в виде раствора соли, в наборах
1) Zn и Pb(NO 3) 2
2) Cu и Hg(NO 3) 2
3) Со и MnSO 4
16–17. Коррозия стального изделия, склепанного с
16. хромом
17. никелем
во влажном воздухе
1) усиливается
2) ослабевает
3) не изменяется
4) не знаю
7. Неметаллы главных подгрупп IV–VII групп
Водород
Водород – первый элемент Периодической системы (1‑й период, порядковый номер 1). Не имеет полной аналогии с остальными химическими элементами и не принадлежит ни к какой группе (в таблицах условно помещается в IA– и/или в VIIA‑группу).
Атом водорода наименьший по размерам и самый легкий среди атомов всех элементов. Электронная формула атома 1s 1 , характерные степени окисления 0, +I и реже – I. Состояние H I считается устойчивым (соединения с H ‑I – сильные восстановители).
Шкала степеней окисления водорода:

По электроотрицательности (2,10) водород занимает промежуточное положение между типичными металлами и типичными неметаллами. Проявляет амфотерные свойства – металлические и неметаллические. Входит в состав катионов (катионы оксония Н 3 O + и аммония NH 4+ , аквакатионы металлов) и многочисленных анионов – кислых кислотных остатков (HS ‑ , HCO 3 ‑ и др.).
Природный водород содержит изотоп 1Н – протий с примесью стабильного изотопа 2 H(D) – дейтерия и следами радиоактивного изотопа 3 Н(Т) – трития (на Земле всего 2 кг трития). В химии символом Н в формулах веществ обозначается содержащаяся в них природная смесь изотопов с преобладанием изотопа протий, а сами вещества рассматриваются как почти изотопночистые соединения протия.
Водород – наиболее распространенный элемент в космосе (Солнце, большие планеты Юпитер и Сатурн, звезды, межзвездная среда, туманности); в состав космической материи входит 63 % Н, 36 % Не и 1 % всех остальных элементов.
В природе – третий по химической распространенности элемент (после О и Si), основа гидросферы. Встречается в химически связанном виде (вода, живые организмы, нефть, природный уголь, минералы), содержится в верхних слоях атмосферы.
Водород Н 2 . Простое вещество. Бесцветный газ без запаха и вкуса. Молекула содержит ковалентную σ‑связь Н – Н. Очень легкий, термически устойчивый до 2000 °C. Весьма мало растворим в воде. Хемосорбируется металлами Fe, Ni, Pd, Pt, где находится в атомном состоянии.
Водород Н 2 может проявлять в одних условиях восстановительные свойства (чаще), в других – окислительные свойства (реже):
восстановитель Н 2 0 – 2е ‑ = 2Н I
окислитель Н 2 0 + 2е ‑ = 2Н ‑I
Сильный восстановитель при высоких температурах, водород реагирует с неметаллами и оксидами малоактивных металлов, выполняет роль окислителя в реакциях с типичными металлами:
Очень высокой восстановительной способностью обладает атомарный водород Н 0 (водород in statu nascendi, лат., – в момент возникновения), который получают непосредственно в зоне проводимой реакции (время жизни Н 0 0,5 с); например, гранулы магния вносят в подкисленный раствор переманганата калия, протекают реакции:
а) образование атомарного водорода
Mg + 2Н + = Mg 2+ + 2Н 0
б) восстановление перманганат‑иона атомарным водородом
5Н 0 + 3H + + MnO 4 ‑ = Mn 2+ + 4Н 2 O
Другой пример – восстановление нитробензола в анилин (реакция Зинина):
а) Fe + 2Н + = Fe 2+ + 2Н 0
б) C 6 H 5 NO 2 + 6Н 0 = C 6 H 5 NH 2 + 2Н 2 O
Получить атомарный водород можно также пропусканием водорода Н 2 над никелевым катализатором.
Атомарный водород легко восстанавливает при комнатной температуре весьма устойчивые соединения, например KNO 3 и O 2:
2Н 0 (Zn, разб. HCl) + KNO 3 = KNO 2 + H 2 O
2H 0 (Zn, разб. HCl) + O 2 = Н 2 O 2
Аналогично протекают реакции при использовании амфигенов (Zn, Al) в щелочной среде:
а) Zn + 2OH ‑ + 2H 2 O = 2‑ + 2Н 0
б) 8Н 0 + KNO 3 = NH 3 + КОН + 2Н 2 O (кипячение)
Качественная реакция – сгорание собранного в пробирку водорода с «хлопком» («гремучая» смесь с воздухом при содержании Н 2 4–74 % по объему).
Применяется водород как восстановитель и гидрирующий агент в синтезе технически важных продуктов (редкие металлы, NH 3 , НCl, органические вещества).
Вода Н 2 O. Бинарное соединение. Бесцветная жидкость (слой более 5 м толщиной окрашен в голубой цвет), без вкуса и запаха. Молекула имеет строение дважды незавершенного тетраэдра [:: ОН 2 ] (sр 3 ‑гибридизация). Летучее вещество, термически устойчивое до 1000 °C.
В обычных условиях полярные молекулы воды образуют между собой водородные связи. Это обусловливает аномалию температур плавления и кипения воды – они значительно выше, чем у ее химических аналогов (H 2 S и других). Затвердевание воды в лед сопровождается увеличением объема на 9 %, т. е. лед легче жидкой воды (вторая аномалия воды). Наибольшую плотность вода имеет не при 0 °C, а при 4 °C (третья аномалия воды). Твердая вода (лед) легко возгоняется.
Природная вода по изотопному составу водорода в основном 1 Н 2 O с примесью 1 Н 2 НО и 2 Н 2 O, по изотопному составу кислорода в основном Н 2 16 O с примесью Н 2 18 O и Н 2 17 O. В малой степени подвергается диссоциации до Н + , или, точнее, до Н 3 O + , и ОН; очень слабый электролит. Катион оксония Н 3 O + имеет строение незавершенного тетраэдра [: O(Н) 3 ] (sр 3 ‑гибридизация). Образует кристаллогидраты со многими солями, аквакомплексы – с катионами металлов. Реагирует с металлами, неметаллами, оксидами. Вызывает электролитическую диссоциацию кислот, оснований и солей, гидролизует многие бинарные соединения и соли. Подвергается электролизу в присутствии сильных электролитов. Почти универсальный жидкий растворитель неорганических веществ.
Для химических целей природную воду очищают перегонкой (дистиллированная вода), для промышленных целей умягчают, устраняя «временную» и «постоянную» жесткость, или полностью обессоливают, пропуская через иониты в кислотной Н + ‑форме и щелочной ОН ‑ – форме (ионы солей осаждаются на ионитах, а ионы Н + и ОН ‑ переходят в воду и взаимно нейтрализуются). Питьевую воду обеззараживают хлорированием (старый способ) или озонированием (современный, но дорогой способ; озон не только окисляет вредные примеси подобно хлору, но и увеличивает содержание растворенного кислорода).
Уравнения важнейших реакций:

Примеры гидролиза бинарных соединений:
6H 2 O + Al 2 S 3 = 2Al(ОН) 3 ↓ + 3H 2 S
2H 2 O + SF 4 = SO 2 + 4HF (40–60 °C)
6H 2 O + Mg 3 N 2 = 3Mg(OH) 2 ↓ + 2NH 3 (кипячение)
2H 2 O + CaC 2 = Ca(OH) 2 ↓ + C 2 H 2
Вода – окислитель за счет H I:
Электролиз воды:
Электропроводность чистой (дистиллированной) воды весьма мала, поэтому электролиз проводят в присутствии сильных электролитов.
а) в нейтральном растворе (электролит Na 2 SO 4)
катод 2H 2 O + 2е ‑ = H 2 + 2OH
анод 2Н 2 O – 4е ‑ = O 2 + 4H +
раствор ОН ‑ + Н + = Н 2 O
б) в кислом растворе (электролит H 2 SO 4)
катод 2Н + + 2е ‑ = Н 2
анод 2Н 2 O – 4е ‑ = O 2 + 4Н +
в) в щелочном растворе (электролит NaOH)
катод 2Н 2 O + 2е ‑ = Н 2 + 2OН ‑
анод 4OН ‑ – 4е ‑ = O 2 + 2Н 2 O
Один из методов обнаружения воды основан на переходе во влажной атмосфере белого сульфата меди(II) CuSO 4 в голубой медный купорос CuSO 4 5Н 2 O.
Известна изотопная разновидность воды – тяжелая вода D 2 O (2 Н 2 O); в природных водах массовое отношение D 2 O: Н 2 O = 1: 6000.
Плотность, температуры плавления и кипения тяжелой воды выше, чем у обыкновенной. Растворимость большинства веществ в тяжелой воде значительно меньше, чем в обычной воде. Она ядовита, так как замедляет биологические процессы в живых организмах. Тяжелая вода накапливается в остатке электролита при многоразовом электролизе воды. Используется как теплоноситель и замедлитель нейтронов в ядерных реакторах.
Гидрид кальция СаН 2 . Бинарное соединение. Белый, имеет ионное строение Са 2+ (Н ‑) 2 . При плавлении разлагается. Чувствителен к кислороду воздуха. Сильный восстановитель, реагирует с водой, кислотами. Применяется как твердый источник водорода (1 кг СаН 2 дает 1000 л Н 2), осушитель газов и жидкостей, аналитический реагент для количественного определения воды в кристаллогидратах.
Уравнения важнейших реакций:
СаН 2 = Н 2 + Са (особо чистый) (выше 1000 °C)
СаН 2 + 2Н 2 O = Са(ОН) 2 + 2Н 2
СаН 2 + 2НCl (разб.) = СаCl 2 + 2Н 2
СаН 2 + O 2 = Н 2 O + СаО (особо чистый) (300–400 °C)
ЗСаН 2 + N 2 = ЗН 2 + Ca 3 N 2 (выше 1000 °C)
ЗСаН 2 + 2КClO 3 = 2КCl + ЗСаО + ЗН 2 O (450–550 °C)
СаН 2 + H 2 S = CaS + 2Н 2 (500–600 °C)
Получение : обработка нагретого кальция водородом.
Галогены
Хлор. Хлороводород
Хлор – элемент 3‑го периода и VII А‑группы Периодической системы, порядковый номер 17. Электронная формула атома [ 10 Ne]3s 2 3p 5 , характерные степени окисления 0, ‑I, +I, +V и +VII. Наиболее устойчиво состояние Cl ‑I . Шкала степеней окисления хлора:

Хлор обладает высокой электроотрицательностью (2,83), проявляет неметаллические свойства. Входит в состав многих веществ – оксидов, кислот, солей, бинарных соединений.
В природе – двенадцатый по химической распространенности элемент (пятый среди неметаллов). Встречается только в химически связанном виде. Третий по содержанию элемент в природных водах (после О и H), особенно много хлора в морской воде (до 2 % по массе). Жизненно важный элемент для всех организмов.
Хлор Cl 2 . Простое вещество. Желто‑зеленый газ с резким удушливым запахом. Молекула Cl 2 неполярна, содержит σ‑связь CI–Cl. Термически устойчив, негорюч на воздухе; смесь с водородом взрывается на свету (водород сгорает в хлоре):
Хорошо растворим в воде, подвергается в ней дисмутации на 50 % и полностью – в щелочном растворе:

Раствор хлора в воде называют хлорной водой, на свету кислота НClO разлагается на НCl и атомарный кислород О 0 , поэтому «хлорную воду» надо хранить в темной склянке. Наличием в «хлорной воде» кислоты НСlO и образованием атомарного кислорода объясняются ее сильные окислительные свойства: например, во влажном хлоре обесцвечиваются многие красители.
Хлор очень сильный окислитель по отношению к металлам и неметаллам:

Реакции с соединениями других галогенов:
а) Cl 2 + 2KBr (p) = 2КCl + Br 2 (кипячение)
б) Cl 2 (нед.) + 2KI (p) = 2КCl + I 2 ↓
3Cl 2 (изб.) + ЗН 2 O + KI = 6НCl + КIO 3 (80 °C)
Качественная реакция – взаимодействие недостатка Cl 2 с KI (см. выше) и обнаружение иода по синему окрашиванию после добавления раствора крахмала.
Получение хлора в промышленности :

и в лаборатории :
4НCl (конц.) + MnO 2 =Cl 2 + MnCl 2 + 2Н 2 O
(аналогично с участием других окислителей; подробнее см. реакции для НCl и NaCl).
Хлор относится к продуктам основного химического производства, используется для получения брома и иода, хлоридов и кислородсодержащих производных, для отбеливания бумаги, как дезинфицирующее средство для питьевой воды. Ядовит.
Хлороводород НCl. Бескислородная кислота. Бесцветный газ с резким запахом, тяжелее воздуха. Молекула содержит ковалентную σ‑связь Н – Cl. Термически устойчив. Очень хорошо растворим в воде; разбавленные растворы называются хлороводородной кислотой, а дымящий концентрированный раствор (35–38 %) – соляной кислотой (название дано еще алхимиками). Сильная кислота в растворе, нейтрализуется щелочами и гидратом аммиака. Сильный восстановитель в концентрированном растворе (за счет Cl ‑I), слабый окислитель в разбавленном растворе (за счет Н I). Составная часть «царской водки».
Качественная реакция на ион Cl ‑ – образование белых осадков AgCl и Hg 2 Cl 2 , которые не переводятся в раствор действием разбавленной азотной кислоты.
Хлороводород служит сырьем в производстве хлоридов, хлорорганических продуктов, используется (в виде раствора) при травлении металлов, разложении минералов и руд.
Уравнения важнейших реакций:
НCl (разб.) + NaOH (разб.) = NaCl + Н 2 O
HCl (разб.) + NH 3 H 2 O = NH 4 Cl + Н 2 O
4HCl (конц., гор.) + МО 2 = МCl 2 + Cl 2 + 2H 2 O (М = Mn, Pb)
16HCl (конц., гор.) + 2КMnO 4(т) = 2MnCl 2 + 5Cl 2 + 8H 2 O + 2КCl
14HCl (конц.) + К 2 Cr 2 O 7(т) = 2CrCl 3 + ЗCl 2 + 7H 2 O + 2КCl
6HCl (конц.) + КClO 3(т) = КCl + ЗCl 2 + 3H 2 O (50–80 °C)
4HCl (конц.) + Са(ClO) 2(т) = СаCl 2 + 2Cl 2 | + 2Н 2 O
2HCl (разб.) + М = МCl 2 + H 2 (М = Fe, Zn)
2HCl (разб.) + МСO 3 = МCl 2 + СO 2 + H 2 O (М = Са, Ва)
HCl (разб.) + AgNO 3 = HNO 3 + AgCl↓
Получение НCl в промышленности – сжигание Н 2 в Cl 2 (см.), в лаборатории – вытеснение из хлоридов серной кислотой:
NaCl (т) + H 2 SO 4 (конц.) = NaHSO 4 + НCl (50 °C)
2NaCl (т) + H 2 SO 4 (конц.) = Na 2 SO 4 + 2НCl (120 °C)
Хлориды
Хлорид натрия NaCl. Бескислородная соль. Бытовое название поваренная соль. Белый, слабогигроскопичный. Плавится и кипит без разложения. Умеренно растворим в воде, растворимость мало зависит от температуры, раствор имеет характерный соленый вкус. Гидролизу не подвергается. Слабый восстановитель. Вступает в реакции ионного обмена. Подвергается электролизу в расплаве и растворе.
Применяется для получения водорода, натрия и хлора, соды, едкого натра и хлороводорода, как компонент охлаждающих смесей, пищевой продукт и консервирующее средство.
В природе – основная часть залежей каменной соли, или галита, и сильвинита (вместе с КCl), рапы соляных озер, минеральных примесей морской воды (содержание NaCl = 2,7 %). В промышленности получают выпариванием природных рассолов.
Уравнения важнейших реакций:
2NaCl (т) + 2H 2 SO 4 (конц.) + MnO 2(т) = Cl 2 + MnSO 4 + 2Н 2 O + Na 2 SO 4 (100 °C)
10NaCl (т) + 8H 2 SO 4 (конц.) + 2КMnO 4(т) = 5Cl 2 + 2MnSO 4 + 8Н 2 O + 5Na 2 SO 4 + K 2 SO 4 (100 °C)
6NaCl (т) + 7H 2 SO 4 (конц.) + К 2 Cr 2 O 7(т) = ЗCl 2 + Cr 2 (SO 4) 3 + 7Н 2 O + 3Na 2 SO 4 + K 2 SO 4 (100 °C)
2NaCl (т) + 4H 2 SO 4 (конц.) + РЬO 2(т) = Cl 2 + Pb(HSO 4) 2 + 2Н 2 O + 2NaHSO 4 (50 °C)
NaCl (разб.) + AgNO 3 = NaNO 3 + AgCl↓

Хлорид калия KCl. Бескислородная соль. Белый, негигроскопичный. Плавится и кипит без разложения. Умеренно растворим в воде, раствор имеет горький вкус, гидролиза нет. Вступает в реакции ионного обмена. Применяется как калийное удобрение, для получения К, КОН и Cl 2 . В природе основная составная часть (наравне с NaCl) залежей сильвинита.
Уравнения важнейших реакций одинаковы с таковыми для NaCl.
Хлорид кальция СаCl 2 . Бескислородная соль. Белый, плавится без разложения. Расплывается на воздухе за счет энергичного поглощения влаги. Образует кристаллогидрат СаCl 2 6Н 2 O с температурой обезвоживания 260 °C. Хорошо растворим в воде, гидролиза нет. Вступает в реакции ионного обмена. Применяется для осушения газов и жидкостей, приготовления охлаждающих смесей. Компонент природных вод, составная часть их «постоянной» жесткости.
Уравнения важнейших реакций:
СаCl 2(т) + 2H 2 SO 4 (конц.) = Ca(HSO 4) 2 + 2НCl (50 °C)
СаCl 2(т) + H 2 SO 4 (конц.) = CaSO 4 ↓ + 2НCl (100 °C)
СаCl 2 + 2NaOH (конц.) = Ca(OH) 2 ↓ + 2NaCl
ЗСаCl 2 + 2Na 3 PO 4 = Са 3 (РO 4) 2 ↓ + 6NaCl
СаCl 2 + К 2 СO 3 = СаСO 3 ↓ + 2КCl
СаCl 2 + 2NaF = CaF 2 ↓ + 2NaCl
Получение:
СаСO 3 + 2HCl = СаCl 2 + СO 3 + Н 2 O
Хлорид алюминия AlCl 3 . Бескислородная соль. Белый, легкоплавкий, сильнолетучий. В паре состоит из ковалентных мономеров AlCl 3 (треугольное строение, sр 2 ‑гибридизация, преобладают при 440–800 °C) и димеров Al 2 Cl 6 (точнее, Cl 2 AlCl 2 AlCl 2 , строение – два тетраэдра с общим ребром, sр 3 ‑гибридизация, преобладают при 183–440 °C). Гигроскопичен, на воздухе «дымит». Образует кристаллогидрат, разлагающийся при нагревании. Хорошо растворим в воде (с сильным экзо ‑эффектом), полностью диссоциирует на ионы, создает в растворе сильнокислотную среду вследствие гидролиза. Реагирует со щелочами, гидратом аммиака. Восстанавливается при электролизе расплава. Вступает в реакции ионного обмена.
Качественная реакция на ион Al 3+ – образование осадка AlРO 4 , который переводится в раствор концентрированной серной кислотой.
Применяется как сырье в производстве алюминия, катализатор в органическом синтезе и при крекинге нефти, переносчик хлора в органических реакциях. Уравнения важнейших реакций:

Получение AlCl 3 в промышленности – хлорирование каолина, глинозёма или боксита в присутствии кокса:
Al 2 O 3 + ЗС (кокс) + ЗCl 2 = 2AlCl 3 + ЗСО (900 °C)
Хлорид железа(Н) FeCl 2 . Бескислородная соль. Белый (гидрат голубовато‑зеленый), гигроскопичный. Плавится и кипит без разложения. При сильном нагревании летуч в потоке HCl. Связи Fe – Cl преимущественно ковалентные, пар состоит из мономеров FeCl 2 (линейное строение, sp‑гибридизация) и димеров Fe 2 Cl 4 . Чувствителен к кислороду воздуха (темнеет). Хорошо растворим в воде (с сильным экзо ‑эффектом), полностью диссоциирует на ионы, слабо гидролизуется по катиону. При кипячении раствора разлагается. Реагирует с кислотами, щелочами, гидратом аммиака. Типичный восстановитель. Вступает в реакции ионного обмена и комплексообразования.
Применяется для синтеза FeCl 3 и Fe 2 O 3 , как катализатор в органическом синтезе, компонент лекарственных средств против анемии.
Уравнения важнейших реакций:

Получение: взаимодействие Fe с соляной кислотой:
Fe + 2НCl =FeCl 2 + Н 2
(в промышленности используют хлороводород и ведут процесс при 500 °C).
Хлорид железа(III) FeCl 3 . Бескислородная соль. Черно‑коричневый (темно‑красный в проходящем свете, зеленый в отраженном), гидрат темно‑желтый. При плавлении переходит в красную жидкость. Весьма летуч, при сильном нагревании разлагается. Связи Fe – Cl преимущественно ковалентные. Пар состоит из мономеров FeCl 3 (треугольное строение, sр 2 ‑гибридизация, преобладают выше 750 °C) и димеров Fe 2 Cl 6 (точнее, Cl 2 FeCl 2 FeCl 2 , строение – два тетраэдра с общим ребром, sр 3 ‑гибридизация, преобладают при 316–750 °C). Кристаллогидрат FeCl 3 6Н 2 O имеет строение Cl 2Н 2 O. Хорошо растворим в воде, раствор окрашен в желтый цвет; сильно гидролизован по катиону. Разлагается в горячей воде, реагирует со щелочами. Слабый окислитель и восстановитель.
Применяется как хлорагент, катализатор в органическом синтезе, протрава при крашении тканей, коагулянт при очистке питьевой воды, травитель медных пластин в гальванопластике, компонент кровоостанавливающих препаратов.
Уравнения важнейших реакций:

Хлорид аммония NH 4 Cl. Бескислородная соль, техническое название нашатырь. Белый, летучий, термически неустойчивый. Хорошо растворим в воде (с заметным эндо ‑эффектом, Q = ‑16 кДж), гидролизуется по катиону. Разлагается щелочами при кипячении раствора, переводит в раствор магний и гидроксид магния. Вступает в реакцию конмутации с нитратами.
Качественная реакция на ион NH 4 + – выделение NH 3 при кипячении со щелочами или при нагревании с гашёной известью.
Применяется в неорганическом синтезе, в частности для создания слабокислотной среды, как компонент азотных удобрений, сухих гальванических элементов, при пайке медных и лужении стальных изделий.
Уравнения важнейших реакций:

Получение: взаимодействие NH 3 с HCl в газовой фазе или NH 3 Н 2 O с HCl в растворе.
Гипохлориты. Хлораты
Гипохлорит кальция Са(СlO) 2 . Соль хлорноватистой кислоты HClO. Белый, при нагревании разлагается без плавления. Хорошо растворим в холодной воде (образуется бесцветный раствор), гидролизуется по аниону. Реакционноспособный, полностью разлагается горячей водой, кислотами. Сильный окислитель. При стоянии раствор поглощает углекислый газ из воздуха. Является активной составной частью хлорной (белильной) извести – смеси неопределенного состава с СаCl 2 и Са(ОН) 2 . Уравнения важнейших реакций:
Са(ClO) 2 = СаCl 2 + O 2 (180 °C)
Са(ClO) 2(т) + 4НCl (конц.) = СаCl 2 + 2Cl 2 + 2Н 2 O (80 °C)
Са(ClO) 2 + Н 2 O + СO 2 = СаСO 3 ↓ + 2НClO (на холоду)
Са(ClO) 2 + 2Н 2 O 2 (разб.) = СаCl 2 + 2Н 2 O + 2O 2
Получение:
2Са(ОН) 2 (суспензия) + 2Cl 2(г) = Са(ClO) 2 + СаCl 2 + 2Н 2 O
Хлорат калия КСlO 3 . Соль хлорноватой кислоты НСlO 3 , наиболее известная соль кислородсодержащих кислот хлора. Техническое название – бертоллетова соль (по имени ее первооткрывателя К.‑Л. Бертолле, 1786). Белый, плавится без разложения, при дальнейшем нагревании разлагается. Хорошо растворим в воде (образуется бесцветный раствор), гидролиза нет. Разлагается концентрированными кислотами. Сильный окислитель при сплавлении.
Применяется как компонент взрывчатых и пиротехнических смесей, головок спичек, в лаборатории – твердый источник кислорода.
Уравнения важнейших реакций:
4КClO 3 = ЗКClO 4 + КCl (400 °C)
КClO 3(т) + 6НCl (конц.) = КCl + ЗCl 2 | + ЗН 2 O (50–80 °C)
ЗКClO 3(т) + 2H 2 SO 4 (конц., гор.) = 2ClO 2 | + КClO 4 + Н 2 O + 2KHSO 4
(диоксид хлора на свету взрывается: 2ClO 2(г) = Cl 2 + 2O 2)
2КClO 3 + Е 2 (изб.) = 2КЕO 3 + Cl 2 (в разб. HNO 3 , Е = Br, I)
Получение КClO 3 в промышленности – электролиз горячего раствора КCl (продукт КClO 3 выделяется на аноде):
Бромиды. Иодиды
Бромид калия КBr. Бескислородная соль. Белый, негигроскопичный, плавится без разложения. Хорошо растворим в воде, гидролиза нет. Восстановитель (более слабый, чем KI).
Качественная реакция на ион Br – вытеснение брома из раствора КBr хлором и экстракция брома в органический растворитель, например СCl 4 (в результате водный слой обесцвечивается, органический слой окрашивается в бурый цвет).
Применяется как компонент травителей при гравировке по металлам, составная часть фотоэмульсий, лекарственное средство.
Уравнения важнейших реакций:

Получение:
K 2 CO 3 + 2HBr = 2KBr + CO 2 + H 2 O
Иодид калия KI. Бескислородная соль. Белый, негигроскопичный. При хранении на свету желтеет. Хорошо растворим в воде, гидролиза нет. Типичный восстановитель. Водный раствор KI хорошо растворяет I 2 за счет комплексообразования.
Качественная реакция на ион I – вытеснение иода из раствора KI недостатком хлора и экстракция иода в органический растворитель, например СCl 4 (в результате водный слой обесцвечивается, органический слой окрашивается в фиолетовый цвет).
Уравнения важнейших реакций:

Получение:
K 2 CO 3 + 2HI = 2KI + СO 2 + Н 2 O
Халькогены
Кислород
Кислород – элемент 2‑го периода и VIA‑группы Периодической системы, порядковый номер 8, относится к халькогенам (но чаще рассматривается отдельно). Электронная формула атома [ 2 He]2s 2 2p 4 , характерные степени окисления чаще 0 и – II, реже – I и +II, состояние О II считается устойчивым.
Шкала степеней окисления кислорода:

Кислород обладает высокой электроотрицательностью (3,50, второй элемент после фтора), проявляет типичные неметаллические свойства. Образует соединения со всеми элементами, кроме Не, Ne и Ar, входит в состав многочисленных оксидов, гидроксидов, солей кислородсодержащих кислот.
Природный кислород содержит изотоп 16 O с примесью изотопов 17 O и 18 O. В химии большинство соединений природного кислорода рассматривается как изотопно‑чистые соединения кислорода‑16.
Кислород – самый распространенный элемент в земной коре (55 %) и природных водах, встречается в свободном и связанном виде. Жизненно важный элемент для всех организмов.
Кислород O 2 . Простое вещество. Состоит из неполярных молекул О 2 (дикислород ) с σπ‑связью O=O, устойчивая аллотропная форма существования элемента в свободном виде. Бесцветный газ, в жидком состоянии – светло‑голубой, в твердом – синий.
Составная часть воздуха: 20,94 % по объему, 23,13 % по массе. Из жидкого воздуха кислород выкипает после азота N 2 . Малорастворим в воде (31 мл/1 л Н 2 O при 20 °C), но несколько лучше, чем N 2 . При комнатной температуре обладает малой химической активностью из‑за прочности двойной связи в молекулах.
Кислород поддерживает горение многих веществ. Сильный окислитель при высоких температурах, реагирует с большинством металлов и неметаллов:

Кислород вызывает ржавление (медленное окисление) железа, уравнения реакций см. в 11.3. Особенно активен атомарный кислород О 0 (активность выше, чем у озона O 3), обычно получаемый непосредственно в зоне реакции при термическом разложении многих веществ.
Простейшая качественная реакция – яркое загорание тлеющей древесной лучинки в атмосфере кислорода.
Получение кислорода:
а) в промышленности – фракционная дистилляция жидкого воздуха, электролиз воды (уравнения реакций см. в разд. 12);
б) в лаборатории – нагревание легко разлагающихся кислородсодержащих веществ:
2HgO = 2Hg + O 2 (450–500 °C)
2КMnO 4 = К 2 MnO 4 + MnO 2 + O 2 (200–240 °C)
2Na 2 O 2 = 2Na 2 O + O 2 (400–675 °C, вакуум)
2КClO 3 = 2КCl + 3O 2 (150–300 °C, кат. MnO 2)
2KNO 3 = 2KNO 2 + O 2 (400–520 °C)
Кислород является важнейшим продуктом основного химического производства. Применяется как реагент в химической технологии (обжиг сульфидных руд, синтез оксидов), металлургии (производство чугуна и стали) и газификации природного угля, при сварке и резке металлов; жидкий кислород – окислитель топлива в ракетной технике.
Убыль кислорода в атмосфере в результате процессов горения, гниения и дыхания возмещается растениями при фотосинтезе. При вдыхании человеком и животными воздуха в легкие кислород связывается с гемоглобином крови и переносится в клетки, где органические вещества (в первую очередь глюкоза) с его помощью окисляются и обеспечивают жизненную энергию организмов.
Озон O 3 . Простое вещество (трикислород), неустойчивая аллотропная форма существования элемента. Светло‑синий газ с характерным («озоновым») запахом, тяжелее воздуха. Молекула имеет строение незавершенного треугольника [: O(O) 2 ] (sр 2 ‑гибридизация, валентный угол 117°), содержит ковалентные σπ‑связи O=O. Разлагается под действием ультрафиолетового излучения, катализаторов и оксидов азота (разрушение озонового слоя атмосферы Земли). Устойчив в смеси с O 2 (озонированный кислород). Малорастворим в воде (285 мл/1 л Н 2 O), но значительно лучше, чем O 2 . Сильный окислитель (более сильный, чем O 2 , но более слабый, чем атомарный кислород O 0). Окисляет при комнатной температуре многие металлы и неметаллы до высоких степеней окисления. С надпероксидами щелочных металлов (К, Rb, Cs) образует оранжево‑красные озониды. Не реагирует с Au, Cu, Ni, Pt, Sn. Генерируется из кислорода O 2 в специальном приборе – озонаторе.
Качественная реакция – выделение иода из раствора KI при комнатной температуре (O 2 в реакцию не вступает). Уравнения важнейших реакций:

Получение : под действием электрического разряда в озонаторе:
Применяется для дезинфекции питьевой воды, при отбеливании тканей и минеральных масел, как реагент в
неорганическом и органическом синтезе. В атмосфере Земли озоновый слой (на высоте =25 км) защищает живой мир от воздействия космического ультрафиолетового излучения.
Атомарный кислород О 0 . Третья аллотропная форма кислорода. Более сильный окислитель по сравнению с O 2 и O 3 . Образуется при распаде молекул O 2 и O 3 под действием ультрафиолетового излучения. Возникает при термическом разложении кислородсодержащих веществ (см. выше, получение O 2); при отсутствии восстановителей тут же переходит снова в O 2 и O 3 , в присутствии восстановителей окисляет их:
KNO 3 = KNO 2 + O 0
О 0 + С (графит) = СO 2
Поэтому вещества, легко отщепляющие кислород при нагревании, проявляют сильные окислительные свойства.
Пероксид водорода Н 2 O 2 . Бинарное соединение. Молекула Н 2 O 2 неплоская, имеет строение с σ‑связью О – О на ребре и связями Н – О на плоскостях двугранного угла. Степень окисления кислорода равна – I. Группа – О – О– называется пероксогруппой.

Бесцветная жидкость, вязкая, тяжелее воды, чувствительна к свету и примесям (стабилизатор Н 3 РO 4). Разлагается со взрывом при слабом нагревании, на катализаторе – при комнатной температуре. Неограниченно смешивается с водой. Разбавленными щелочами нейтрализуется не полностью. Сильный окислитель, слабый восстановитель.
Пероксид водорода применяется как отбеливатель текстиля, бумаги, кож, жиров и минеральных масел, окислитель ракетного топлива, реагент в органическом синтезе, при осветлении картин старых мастеров (потемневший красочный слой из‑за перехода белил – гидроксокарбонатов свинца – в черный PbS осветляют переводом в белый PbSO 4). В промышленности обычно используют взрывобезопасный 30 %‑ный раствор Н 2 O 2 (пергидроль), в медицине – 3 %‑ный раствор.
Уравнения важнейших реакций:
2Н 2 O 2 = 2Н 2 O + O 2 (выше 150 °C или на кат. MnO 2)
Н 2 O 2 (разб.) + NaOH (разб.) = NaHO 2 + Н 2 O
Н 2 O 2 (конц.) + 2NaOH (т) = Na 2 O 2 ↓ + 2H 2 O (0 °C)
Н 2 O 2 (3 %) + 2H + + 2I ‑ = I 2 ↓ + 2Н 2 O
5Н 2 O 2 (30 %) + I 2(т) = 2НIO 3 + 4Н 2 O
Н 2 O 2 (10 %) + SO 3 2‑ = SO 3 2‑ + H 2 O
4Н 2 O 2 (30 %) + PbS (черн.) = 4H 2 O + PbSO 4 (бел.)↓
3H 2 O 2 + 2 3‑ = 2CrO 4 2‑ + 8H 2 O + 2OH ‑
2Н 2 O 2 (конц.) + Са(ClO) 2 = СаCl 2 + 2Н 2 O + 2O 2
5H 2 O 2 + 6H + + 2MnO 4 ‑ = 2Mn 2+ + 5O 2 + 8Н 2 O
Получение : в лаборатории